- Головна
- /
- Статті
- /
- Ендокринологія. Цукровий діабет
- /
- Субклінічний гіпотиреоз: стан проблеми та підходи до лікування
Субклінічний гіпотиреоз: стан проблеми та підходи до лікування
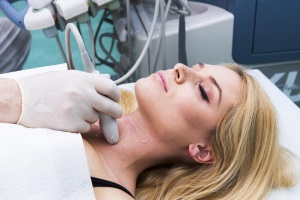
Протягом останнього десятиліття в клінічній практиці широко застосовуються радіоімунологічні методи визначення в плазмі крові тиреотропного гормону (ТТГ) гіпофіза та рівня гормонів щитоподібної залози (ЩЗ), що відкрило нову еру в діагностиці та лікуванні гіпотиреозу.
Це дало змогу не лише вірогідно розмежувати підвищений, нормальний чи знижений рівні ТТГ у крові й тим самим верифікувати стани гіпо-, еу- та гіпертиреозу, а й діагностувати порушення функції ЩЗ, що перебігають латентно, а саме – субклінічний гіпотиреоз. Під цим терміном розуміємо клінічний синдром, при якому визначаються нормальні показники гормонів ЩЗ у поєднанні з підвищеним рівнем ТТГ.
 Проблема прихованих порушень функції ЩЗ є порівняно новою, адже вона значною мірою зумовлена запровадженням зазначених методів функціональної діагностики. Однак за даними досліджень різних авторів, частота субклінічного гіпотиреозу становить у середньому 6% загальної популяції, що у 5-6 разів перевищує поширеність явного гіпотиреозу. На сьогодні у світі питання субклінічного гіпотиреозу як досить поширеного патологічного стану активно обговорюється в численних публікаціях і виступах на наукових форумах. Недаремно у Міжнародній класифікації захворювань 10-го перегляду субклінічний гіпотиреоз виділено в окрему рубрику.
Проблема прихованих порушень функції ЩЗ є порівняно новою, адже вона значною мірою зумовлена запровадженням зазначених методів функціональної діагностики. Однак за даними досліджень різних авторів, частота субклінічного гіпотиреозу становить у середньому 6% загальної популяції, що у 5-6 разів перевищує поширеність явного гіпотиреозу. На сьогодні у світі питання субклінічного гіпотиреозу як досить поширеного патологічного стану активно обговорюється в численних публікаціях і виступах на наукових форумах. Недаремно у Міжнародній класифікації захворювань 10-го перегляду субклінічний гіпотиреоз виділено в окрему рубрику.
На сьогодні залишається дискусійним питання щодо терапевтичного підходу при субклінічному гіпотиреозі: активно втручатися призначенням адекватних доз замісної терапії чи динамічно спостерігати за такими пацієнтами. Як із теоретичних, так і практичних позицій саме ця проблема заслуговує на особливу увагу.
Що таке субклінічний гіпертиреоз?
Субклінічний гіпотиреоз – клінічний синдром, зумовлений стійким пограничним зниженням рівня гормонів ЩЗ в організмі, при якому визначається нормальний рівень тиреоїдних гормонів у поєднанні з помірно підвищеним рівнем ТТГ.
У 1967 р. P. Bastenie зі співавт. запропонували терміни «латентний гіпотиреоз» або «преклінічна мікседема» для хворих із рівнем зв'язаного з білком йоду в крові на нижній межі норми і наявністю антитиреоїдних антитіл. На сьогодні загальноприйнятим терміном вважають «субклінічний гіпотиреоз», що позначає граничний стан між нормою і клінічно явною формою первинного гіпотиреозу. Субклінічний гіпотиреоз характеризується підвищеним рівнем ТТГ у крові при нормальному вмісті загальних і вільних тиреоїдних гормонів, насамперед вільного Т4, безсимптомним перебігом або з мінімальними проявами тиреоїдної недостатності. У визначенні діагностичних критеріїв дискусійними залишаються питання:
- Чи свідчить про субклінічний гіпотиреоз будь-яке перевищення верхньої межі норми вмісту ТТГ у крові чи лише значне – понад 10 мМО/л?
- Чи варто відносити до субклінічного гіпотиреозу випадки з нормальним базальним рівнем ТТГ і підвищеним стимульованим рівнем у відповідь на введення тиреотропін-рилізинг-гормону (ТРГ) (так званий біохімічний гіпотиреоз)?
Слід зазначити, що застосування високочутливих методів визначення ТТГ знизило потребу в проведенні стимулюючої проби з ТРГ, хоча й не замінило її повністю. Так, J. Haggerty і A. Prange, застосовуючи термін «граничний гіпотиреоз», вважають його діагностичним критерієм підвищену реакцію ТТГ на ТРГ; при цьому базальний рівень ТТГ може бути як підвищеним, так і нормальним при нормальному вмісті тиреоїдних гормонів у крові. Подібний погляд викладено в огляді J. Griffin. Автор звертає увагу на той факт, що рівень ТТГ у хворих на субклінічний гіпотиреоз, зазвичай, перебуває у межах 20 мМО/л, а вищі значення відповідають клінічно явному гіпотиреозу.
Оскільки підвищений вміст ТТГ у крові є основним діагностичним критерієм субклінічного гіпотиреозу, з метою уникнення гіпердіагностики цієї патології у літературі розглядаються інші можливі причини гіперсекреції ТТГ. Так, протягом 48 годин після пологів у новонародженого відбувається фізіологічний викид ТТГ, як правило, у межах 20 мМО/л, що, очевидно, пов'язано з охолодженням.
Антагоністи дофаміну метоклопрамід, сульпірид можуть призводити до підвищення ТТГ у крові шляхом порушення впливу дофаміну на секрецію ТТГ. Аміодарон, підвищуючи в крові рівень загального і вільного Т4, в деяких хворих може спричинити незначне підвищення рівня ТТГ на початку лікування (до 3 місяців), а стимульований рівень у пробі з ТРГ підвищується досить часто. Вважають, що аміодарон конкурентно пригнічує зв'язування Т3 з ядерними рецепторами тиреотрофів гіпофіза. Разом із тим аміодарон як препарат із високим умістом йоду може спричинити йодоіндукований первинний гіпотиреоз (як, зрештою, і йодоіндукований тиреотоксикоз).
Незначне підвищення рівня ТТГ (до 10 мМО/л) у поєднанні із суттєвим зниженням рівня тиреоїдних гормонів у крові спостерігається у 25% хворих на гіпофізарний і гіпоталамічний гіпотиреоз. Біологічна активність ТТГ у таких випадках знижена.
Резистентність до тиреоїдних гормонів, зумовлена мутацією гена β-рецептора гормонів, може бути генералізованою (клінічно відповідає гіпотиреозу або еутиреозу) або частковою гіпофізарною (клінічно відповідає гіпертиреозу). В обох випадках рівень ТТГ незначно підвищений або нормальний при підвищеному вмісті тиреоїдних гормонів у крові, що і вважається диференційно-діагностичним критерієм.
ТТГ-продукуюча аденома гіпофіза – рідкісна патологія, подібна за біохімічними характеристиками до резистентності до тиреоїдних гормонів. Дослідження крові виявляє у таких хворих підвищений уміст у крові й ТТГ, і тиреоїдних гормонів, а клінічна симптоматика відповідає гіпертиреозу.
У гострій фазі психічних захворювань у 25% хворих протягом перших 2-3 тижнів стаціонарного лікування виявляють підвищені рівні ТТГ і вільного Т4 у крові. Цей стан пояснюють транзиторною активацією гіпоталамо-гіпофізарно-тиреоїдної осі.
Некомпенсований первинний гіпокортицизм у деяких випадках супроводжується підвищенням рівня ТТГ у крові, а під час лікування глюкокортикоїдами спостерігається його нормалізація. Разом із тим слід зважати на можливість поєднаної патології первинних гіпокортицизму й гіпотиреозу (синдрому Шмідта).
У важко хворих людей із різними соматичними захворюваннями, травмами на стадії одужання рівень ТТГ у крові може транзиторно підвищитися (до 20 мМО/л) при нормальному чи зниженому рівні тиреоїдних гормонів. Повторне визначення ТТГ і вільного Т4 у динаміці дає змогу диференціювати цей стан у межах синдрому еутиреоїдної патології від первинного гіпотиреозу.
Для хронічної ниркової недостатності властиве нагромадження в крові метаболітів і лікарських препаратів, що впливають на зв'язування тиреоїдних гормонів і, можливо, їх біологічний ефект. Залежно від медикаментів, що застосовувалися, виявляють як підвищений, так і знижений рівень ТТГ, однак може розвинутися й істинний гіпотиреоз внаслідок затримки в організмі йоду. Наявність гетерофільних антитіл може спричинити підвищення рівня ТТГ у деяких системах його визначення.
Епідеміологія субклінічного гіпотиреозу
За даними різних авторів, показники поширеності субклінічного гіпотиреозу перебувають у межах від 1,2 до 15% залежно від статі й віку обстежених, у середньому – у 6% загальної популяції, що значно перевищує частоту клінічно явного гіпотиреозу (0,3-1,1%).
Субклінічний гіпотиреоз майже втричі частіше спостерігається в жінок, ніж у чоловіків. Якщо серед чоловіків частота субклінічного гіпотиреозу становить 2,8-3%, то серед жінок – 7,5%.
За даними Фремінгемського дослідження з обстежених 892 чоловіків і 1256 жінок віком понад 60 років субклінічний гіпотиреоз було встановлено в 126 (5,9%) пацієнтів, причому серед жінок майже вдвічі частіше (7,7 проти 3,3%).
Під час обстеження 434 чоловіків і 137 жінок віком понад 60 років Р. Drinka і W. Nolten діагностували субклінічний гіпотиреоз у 42 (9,7%) чоловіків і 20 (14,6%) жінок, при тому що маніфестний гіпотиреоз установлено лише в 3 чоловіків і 2 жінок. У всіх пацієнтів із явним гіпотиреозом, а також у 12 (34%) з 35 чоловіків і 12 (67%) з 18 жінок із субклінічним гіпотиреозом відзначено наявність антитиреоїдних антитіл.
В осіб із підвищеним рівнем ТТГ антитіла до ЩЗ виявляють частіше, ніж в осіб із нормальним рівнем ТТГ. За даними різних досліджень субклінічний гіпотиреоз протягом одного року переходить у маніфестний із частотою 7,8-17,8% випадку.
Поширеність субклінічного гіпотиреозу збільшується з віком. Так, у жінок віком понад 40 років частота субклінічного гіпотиреозу становить 4,3%, а у віці 50-60 років – 5,9%. Під час вивчення поширеності гіпотиреозу в пацієнтів віком від 60 до 97 років D.Bemben і співавт. встановили субклінічний гіпотиреоз у 14,6% жінок і 15,4% чоловіків.
За даними класичного 20-річного дослідження, проведеного серед дорослого населення в англійському графстві Вікгем, ризик розвитку гіпотиреозу безпосередньо залежить від початкового рівня ТТГ. Так, ризик виникнення гіпотиреозу протягом наступних 20 років у 40-річних жінок із рівнем ТТГ 2,1 мМО/л становить менше 1% до 50 років. Ризик розвитку маніфестного гіпотиреозу в жінок за умови виявлення в них підвищеного рівня ТТГ у поєднанні зі збільшеним титром антитіл до ЩЗ становить 4,3% на рік, при ізольованому підвищенні рівня ТТГ – 2,6% на рік та ізольованому підвищенні рівня антитиреоїдних антитіл – всього 2,1% на рік.
Діагностика
Діагностику субклінічного гіпотиреозу здійснюють на основі встановлення нормального рівня Т4 і помірно підвищеного рівня ТТГ (від 5,01 до 10 мМО/л при нормі 0,4-5 мМО/л). Рівень Т3 практичного значення для діагностики субклінічного гіпотиреозу не має. Відомо, що при гіпотиреозі спостерігається тенденція до більш пізнього зниження рівня Т3 порівняно з Т4. У частини хворих на гіпотиреоз рівень Т3 може бути навіть дещо підвищеним унаслідок компенсаторної активації дейодування Т4 у біологічно активніший Т3 у периферичних тканинах. Таким чином, необхідним дослідженням для оцінки тиреоїдної функції є визначення рівня ТТГ за допомогою високочутливих методів.
I. Szabolсs і співавт. вивчали частоту субклінічного гіпотиреозу в людей похилого віку, які проживають у регіонах із різним споживанням йоду. Обстежено 346 осіб віком 78-81 рік у регіонах помірної зобної ендемії (Північна Угорщина) з постійним багаторічним споживанням йодованої солі (Словаччина) та достатнім споживанням йоду (Східна Угорщина). За даними цих дослідників, помірний дефіцит йоду в тій чи іншій місцевості не супроводжується збільшенням поширеності субклінічного гіпотиреозу. Частота виявлення підвищеного титру антитиреоїдних антитіл виявилася подібною у трьох регіонах.
P. Perros і співавт. на основі матеріалів обстеження 1310 хворих на цукровий діабет 1 та 2 типів звертають увагу на високу частоту тиреоїдної патології (13,4%), особливо у жінок із діабетом 1 типу (31,4%). Серед захворювань ЩЗ найчастіше спостерігався субклінічний гіпотиреоз, тому автори рекомендують щороку обстежувати хворих на цукровий діабет на предмет виявлення безсимптомної тиреоїдної дисфункції. До подібного висновку дійшли також G. Radetti і співавт. на підставі обстеження 1419 дітей, хворих на цукровий діабет 1 типу, оскільки частота супутнього аутоімунного тиреоїдиту, що нерідко перебігає зі субклінічним гіпотиреозом, досягала 3,9%.
Етіологія й патогенез
Етіологія й патогенез як субклінічного, так і маніфестного гіпотиреозу збігаються, адже під субклінічним гіпотиреозом розуміють мінімально виражену форму саме первинного, а не центрального гіпотиреозу.
Субклінічний гіпотиреоз може розвинутися внаслідок аутоімунного тиреоїдиту за наявності йодної недостатності після резекції ЩЗ, будь-якого виду лікування дифузного токсичного зоба, перенесеного підгострого чи післяпологового тиреоїдиту, зовнішнього опромінення голови чи шиї. Субклінічний гіпотиреоз може бути наслідком застосування деяких медикаментів: аміодарону, йодидів, препаратів літію, інтерферону альфа та інтерлейкіну-2. У той же час уже наявний субклінічний гіпотиреоз може бути не діагностований за вмістом ТТГ у крові хворих, якщо вони отримують дофамінергічні препарати, глюкокортикоїди, а також під час голодування, що справляє інгібуючий ефект на секрецію ТТГ.
Оскільки найчастішою причиною субклінічного гіпотиреозу вважають аутоімунний тиреоїдит, зрозумілим є інтерес до дослідження у цих хворих антитиреоїдних антитіл. Встановлено, що підвищення ТТГ у крові в людей похилого віку певною мірою корелює із наявністю в крові антитиреоїдних антитіл, хоча вони можуть бути відсутніми принаймні в третини хворих. У жінок похилого віку частота виявлення антитиреоїдних антитіл у крові перевищує кількість випадків підвищеного рівня ТТГ, при цьому в кожної третьої жінки з підвищеним рівнем ТТГ антитіла не визначаються.
Зазначене явище відповідає поширеному погляду відносно того, що процес старіння поєднується з появою органоспецифічних і неорганоспецифічних аутоантитіл. У цьому контексті цікавим є дослідження A. Pinchera і співавт., які здійснили порівняльний аналіз частоти виявлення антитиреоїдних антитіл у здорових осіб 50- і 100-річного віку, при цьому відмінності виявилися невірогідними. Проте обстеження госпіталізованих хворих із різною соматичною патологією показали інші результати: у хворих віком від 61 до 95 років антитіла до тиреоглобуліну (ТГ) і мікросомального антигену були наявні в крові значно частіше, ніж у 50-річних. Звідси було зроблено висновок про те, що утворення аутоантитіл до тиреоїдних антигенів тісно пов'язане з наявною соматичною патологією і не належить до проявів старіння. Ці ж автори встановили невисоку частоту антитіл до тиреоїдної пероксидази в людей віком понад 100 років (5,9%) і не виявили в них антитіл до парієтальних клітин шлунка і надниркових залоз. Дослідники вважають, що досягнення віку понад 100 років можливе лише завдяки ефективному функціонуванню імунної системи.
Субклінічний гіпотиреоз може бути спровокований призначенням йодовмісних препаратів (найчастіше аміодарону та йодиду калію) хворим, у минулому лікованим із приводу дифузного токсичного зоба, й препаратів інтерферону альфа переважно з приводу вірусного гепатиту В чи С, особливо в разі наявності в крові антитиреоглобулінових і антимікросомальних антитіл.
З огляду на це особливий інтерес становить дослідження W. Reinhardt і співавт., під час якого 40 еутиреоїдним хворим із аутоімунним тиреоїдитом, які проживають в умовах незначної йодної ендемії, протягом 2-13 місяців (у середньому – 4 міс.) призначали йодид калію у добовій дозі 250 мкг. До контрольної групи увійшло 43 хворих. У групі, що отримувала йодид калію, у 7 пацієнтів розвинувся субклінічний гіпотиреоз, в 1 – явний гіпотиреоз і в 1 – гіпертиреоз із появою у крові імуноглобулінів, що інгібують зв'язування ТТГ. Після припинення прийому йодиду калію тиреоїдна функція нормалізувалася в 3 хворих зі субклінічним гіпотиреозом і в одного пацієнта з гіпертиреозом. У контрольній групі субклінічний гіпотиреоз розвинувся лише в 1 із 43 хворих. Автори звертають увагу на той факт, що призначення йодиду калію хворим на аутоімунний тиреоїдит призводило до незначних, але вірогідних порушень тиреоїдної функції. Описано, що навіть фарба для волосся, що містить високу концентрацію йоду, може стати причиною легкої тиреоїдної недостатності у хворих на аутоімунний тиреоїдит.
N. Linder і співавт. засвідчили, що розвиток субклінічного гіпотиреозу нерідко може провокуватися зовнішнім застосуванням йодовмісних антисептиків у недоношених дітей на відміну від антисептиків, що містять хлоргексидин. Встановлено вірогідну позитивну кореляцію рівня ТТГ у крові з площею дезінфекції йодовмісними антисептиками.
На сьогодні відсутні однозначні дані про те, що запровадження масової йодної профілактики супроводжується збільшенням поширеності аутоімунних тиреопатій і гіпотиреозу і що в регіонах із помірним йодним дефіцитом аутоімунні тиреопатії менш поширені, ніж у регіонах із достатнім споживанням йоду.
Так, у великому популяційному дослідженні Р. Laurberg і співавт. вивчали структуру тиреоїдної патології у населення похилого віку Ютландії у Данії (регіон помірного йодного дефіциту; медіана йодурії – 38 мкг/л) та Ісландії (регіон із достатнім йодним забезпеченням; медіана йодурії – 150 мкг/л), при цьому частота підвищеного титру антитиреоїдних антитіл виявилася вдвічі вищою у йододефіцитній Ютландії.
На думку деяких авторів, паління може пришвидшити маніфестацію гіпотиреозу у хворих із наявністю антитиреоїдних антитіл. В.Мuller і співавт. з'ясували, що у жінок, які палять, рівень ТТГ у середньому значно вищий (21,3±16,6 мМО/л проти 12,7±7,2 мМО/л), ніж у жінок, які не палять, у яких до того ж визначається вищий рівень загальних ліпідів і ліпопротеїнів низької щільності (ЛПНЩ) – на 16 і 28% відповідно. Негативний вплив паління пояснюють дією на ЩЗ тіоціанату, давно відомого своїм зобогенним ефектом; нікотин, як виявилося, не здійснює істотного впливу на функціональний стан залози.
Серед інших причин розвитку субклінічного гіпотиреозу слід зазначити раніше перенесену операцію на ЩЗ або лікування радіоактивним йодом із приводу тиреотоксикозу. Частота розвитку гіпотиреозу після операції повністю залежить від об'єму хірургічного втручання. Встановлено чітку закономірність між об'ємом тиреоїдного залишку, рівнем тиреоїдних гормонів і ТТГ.
В.В. Кучер й А.М. Карякін вивчали віддалені наслідки операцій на ЩЗ протягом 8 років. У 16,5% із 313 пацієнтів, оперованих із приводу дифузного токсичного зоба (ДТЗ), було виявлено субклінічний гіпотиреоз. Це підтверджує і робота Ю.Б. Кирилова і співавт., які діагностували субклінічний гіпотиреоз у віддаленому післяопераційному періоді в 11% із 164 прооперованих пацієнтів із ДТЗ. В. Вusnardo і співавт. описали віддалені наслідки хірургічного лікування ДТЗ у 93 пацієнтів за період 1973-1980 рр. Через 3 роки субклінічний гіпотиреоз було діагностовано у 22% пацієнтів, а через 6 років – лише у 9%.
S. Turner і співавт. показали, що субклінічний гіпотиреоз розвинувся в 9,5% із 84 пацієнтів, яким 5 років перед тим було проведено радіотерапію з приводу злоякісної пухлини голови й шиї. D. Liening і співавт. здійснили порівняльний аналіз частоти розвитку субклінічного гіпотиреозу в пацієнтів після радіотерапії з приводу злоякісної пухлини голови й шиї та комбінованого лікування (хірургічне втручання й радіотерапія). Результати були такими: субклінічний гіпотиреоз встановлено в 26% пацієнтів після радіотерапії та в 65% – після комбінованого лікування.
Клінічні та лабораторно-інструментальні особливості, перебіг субклінічного гіпотиреозу
Під час багаторічного спостереження за особами зі субклінічним гіпотиреозом виявлено різні варіанти його перебігу. Подібний стан може залишатися стабільним протягом багатьох років. Можливе відновлення нормальної гормонопродукуючої функції ЩЗ (транзиторний субклінічний гіпотиреоз) або прогресування захворювання: гіпотиреоз переходить із субклінічної форми в клінічно явну зі зниженням у крові рівнів загального й вільного Т4.
Транзиторний субклінічний гіпотиреоз може розвинутися після резекції ЩЗ у хворих із підгострим чи післяпологовим тиреоїдитом як одна з фаз захворювання внаслідок лікування йодовмісними та іншими препаратами, що знижують синтез або секрецію тиреоїдних гормонів на тлі наявної тиреоїдної патології. Описано рідкісні випадки відновлення еутиреоїдного стану у хворих на аутоімунний тиреоїдит (АІТ), що пов'язують зі зникненням антитіл до рецептора ТТГ. Подібне явище спостерігається в немовлят із гіпотиреозом, зумовленим трансплацентарним перенесенням від матері антитіл до рецептора ТТГ.
Перехід субклінічного гіпотиреозу до клінічно явного гіпотиреозу відзначається в середньому в 5-15% хворих щороку. Ймовірність прогресування гіпотиреозу залежить від причини його розвитку. Найчастіше це відбувається при АІТ унаслідок зменшення кількості функціонуючих тиреоїдних клітин та їх заміщення лімфоїдними елементами й розвитком фіброзу. Основними прогностичними чинниками вважають наявність у крові антитіл до тиреоїдної пероксидази, а також ступінь підвищення базального рівня ТТГ. За даними M. Helfand і L. Grapo, в групі хворих на субклінічний гіпотиреоз із рівнем ТТГ у крові понад 10 мМО/л і наявністю антитиреоїдних антитіл явний гіпотиреоз розвивався в 7% на рік, а в групі хворих із рівнем ТТГ понад 14 мМО/л – значно частіше (20% на рік). Найбільшу частоту розвитку явного гіпотиреозу описано в осіб віком понад 65 років із рівнем ТТГ вище 20 мМО/л і титром антимікросомальних антитіл вище 1:1600 – 80% за 4 роки спостереження.
Під час вивчення ехограм ЩЗ у хворих на субклінічний гіпотиреоз, що виник унаслідок АІТ, та з безсимптомним аутоімунним тиреоїдитом частота субклінічного гіпотиреозу виявилася вірогідно вищою в групі з помірним і вираженим зниженнями тиреоїдної ехогенності порівняно з групою із нормальною та трохи зниженою ехогенністю (70,4 проти 23,0%). За наступний рік спостереження гіпотиреоз розвинувся у хворих зі зниженою ехогенністю. Автори вважають ступінь зниження ехогенності ЩЗ прогностичною ознакою розвитку гіпотиреозу у хворих із безсимптомним АІТ.
Таким чином, субклінічний гіпотиреоз – досить поширений патологічний стан, що розвивається внаслідок різних причин і нерідко впливає на перебіг інших захворювань.
Для субклінічного гіпотиреозу притаманна відсутність явної клінічної симптоматики, однак детальне опитування й цілеспрямоване клінічне обстеження дають змогу виявити в частини хворих ознаки, що відповідають легкій тиреоїдній недостатності: втомлюваність, сухість шкіри, випадіння волосся, мерзлякуватість, закрепи, сонливість, зниження концентрації уваги, депресивний стан. Зазвичай, виражена клінічна симптоматика відсутня або неспецифічна. Проте в 25-50% пацієнтів спостерігаються помірні, але притаманні для гіпотиреозу ознаки. При субклінічному гіпотиреозі відзначаються порушення з боку багатьох органів і систем.
Вивченню питання впливу субклінічного гіпотиреозу на стан серцево-судинної системи й ліпідний обмін присвячено велику кількість досліджень. Під час деяких із них у пацієнтів зі субклінічним гіпотиреозом відзначали подовження систолічних часових інтервалів, на тлі лікування L-тироксином спостерігалася позитивна динаміка, тобто скорочення інтервалів. Для субклінічного гіпотиреозу притаманні й інші кардіоваскулярні розлади: альтерація у систолу, порушення ритму й провідності.
На думку деяких авторів, досить часто єдиним клінічним проявом гіпотиреозу є порушення ритму й провідності, що нерідко «резистентні» до антиаритмічної терапії.
Л.А. Панченкова і співавт. оцінювали стан серцево-судинної системи у хворих на ішемічну хворобу серця (ІХС) із субклінічним гіпотиреозом та еутиреозом. При цьому відзначено більшу кількість епізодів горизонтальної й максимальної глибини депресії сегмента SТ протягом доби у хворих на ІХС зі субклінічним гіпотиреозом порівняно з пацієнтами з еутиреозом (15,3 проти 2,6 і 1,16 проти 0,43 відповідно). Крім того, в групі хворих на ІХС у поєднанні зі субклінічним гіпотиреозом було виявлено ознаки безбольової ішемії міокарда в 50% випадків та істотне підвищення показників діастолічного артеріального тиску.
Біохімічне дослідження крові дає змогу виявити в пацієнтів із субклінічним гіпотиреозом порівняно зі здоровими особами знижений рівень ліпопротеїдів високої щільності (ЛПВЩ), підвищені рівні ЛПНЩ, тригліцеридів, загального холестерину, збільшений індекс атерогенності.
За даними A. Kung і співавт., порушення ліпідного обміну спостерігаються в 50% хворих на субклінічний гіпотиреоз порівняно з 20,8% у контрольній групі (підвищені рівні аполіпопротеїну А1 та В, а також співвідношення рівня загального холестерину до рівня холестерину ЛПВЩ і рівнів ЛПНЩ- і ЛПВЩ-холестерину, рівень ТТГ корелював із співвідношенням рівнів загального холестерину і ЛПВЩ-холестерину). Це дослідження підтверджує несприятливий вплив тиреоїдної недостатності на ліпідний обмін, що підвищує ризик розвитку атеросклерозу.
В.Л. Воронцов і співавт. виявили підвищений рівень ТТГ у 12,56% пацієнтів, які страждають на гіперліпідемію. А. Gupta і R.Sinha встановили підвищений рівень холестерину в пацієнтів зі субклінічним гіпотиреозом порівняно зі здоровими особами (192,13±47,40 і 157,61±37,69 мг/дл відповідно).
За даними D. Pallas і співавт., тест на антитиреоїдні антитіла був позитивним у 22 (25%) з 87 осіб із гіперхолестеринемією порівняно з 5 (6%) у контрольній групі. Крім того, у 8 осіб із гіперхолестеринемією було вперше встановлено субклінічний гіпотиреоз. У пацієнтів зі гіперхолестеринемією рівень ТТГ у середньому був вищим, ніж у контрольній групі, навіть після виключення осіб із підвищеними титрами антитиреоїдних антитіл. Було виявлено позитивну кореляцію між рівнями холестерину й ТТГ.
В.Л. Воронцов і О.И. Смирнова відзначають високий ризик розвитку атеросклерозу при гіпотиреозі в осіб віком 50 років і більше, причому в чоловіків він був вищим, ніж у жінок.
Гіперхолестеринемія при субклінічному гіпотиреозі не піддається лікуванню дієтою, статинами та іншими гіполіпідемічними препаратами, однак при цьому ефективно коригується призначенням препаратів тиреоїдних гормонів.
Крім змін ліпідного обміну, при субклінічному гіпотиреозі виявлено зниження рівня ендотеліальної вазодилатації як маркера раннього атеросклерозу. J. Lekakis і співавт. встановили негативну кореляцію між ендотелійзалежною вазодилатацією і рівнем ТТГ. Вазодилатація була найвищою в осіб із рівнем ТТГ у межах 0,4-2,0 мМО/л, нижчою – при рівні ТТГ від 2,01 до 4,0 мМО/л, ще нижчою – у пацієнтів із субклінічним гіпотиреозом і рівнем ТТГ 4,0-10,0 мМО/л і найнижчою – у пацієнтів із рівнем ТТГ понад 10,0 мМО/л.
Деякі автори знаходять зв'язок між субклінічним гіпотиреозом та ІХС у чоловіків і жінок похилого віку, однак дані S. Miura і співавт. спростовують наявність зв'язку між субклінічним гіпотиреозом, порушенням ліпідного обміну та ІХС. Обстеження 97 хворих на ІХС не виявило відмінностей за рівнем ліпідів між хворими на субклінічний гіпотиреоз і хворими з нормальною тиреоїдною функцією. Хоча в жінок із ІХС рівень тиреоїдних гормонів і ЛПВЩ-холестерину був вірогідно нижчим, автори не встановили впливу субклінічного гіпотиреозу на розвиток ІХС. Якщо хворому на ІХС показана коронарна ангіопластика, супутній субклінічний гіпотиреоз не вважається протипоказанням, оскільки не впливає на результат операції.
Дані літератури підтверджують зв'язок між субклінічним гіпотиреозом і психічними порушеннями.
R. Joffe і А. Levitt обстежували 139 пацієнтів із уніполярною депресією. У 19 з них було діагностовано субклінічний гіпотиреоз. Автори дійшли висновку, що депресія при субклінічному гіпотиреозі відрізняється від депресії в осіб без цієї патології наявністю відчуття паніки й резистентністю до лікування антидепресантами. Дослідження R. Howland підтверджує зв'язок між гіпотиреозом і рефрактерною до лікування депресією. У 52% пацієнтів із депресією, рефрактерною до лікування, було діагностовано субклінічний гіпотиреоз.
R. Kraus і співавт. обстежували хворих на депресією із рівнем ТТГ від середньої величини норми до верхньої її межі. Під час проби з ТРГ реакція ТТГ виявилася підвищеною (дельта ТТГ – понад 25 мМО/л) у 38% хворих на депресію, тому автори дійшли висновку, що субклінічний гіпотиреоз може впливати на розвиток депресії у частини хворих із вищезазначеним базальним ТТГ. Однак приблизно в 25% хворих на депресію описано знижену відповідь ТТГ на ТРГ: дельта ТТГ виявилася меншою 5 мМО/л, але все ж і не такою низькою, як при гіпертиреозі (в останньому випадку – менше 1 мМО/л). Отже, дані тиреоїдних функціональних тестів при депресивних розладах не мають односпрямованого характеру. Можна вважати, що відмінність результатів значною мірою залежить від неоднорідності груп хворих і лікування різними психотропними препаратами. На думку більшості авторів, субклінічний гіпотиреоз не можна вважати причиною розвитку депресії, але він може знижувати поріг для розвитку головних депресивних порушень.
При субклінічному гіпотиреозі відзначається зниження пізнавальної функції, погіршуються пам'ять і увага, явно або приховано знижується інтелект.
F. Моnzani і співавт. у своїх роботах оцінювали нейропсихологічні й поведінкові особливості у хворих на субклінічний гіпотиреоз та в контрольній групі. Під час оцінки за шкалою Векслера автори виявили зниження пам'яті (МQ=89,1±2,9; р=0,002) у пацієнтів зі субклінічним гіпотиреозом. Визначення індексу Кроуна-Кріспа показало незначне розходження за шкалами істерії (р=0,03), занепокоєння (р=0,05), соматичних порушень (р=0,0005) і депресії (р=0,002) у хворих на субклінічний гіпотиреоз і в контрольній групі.
Загалом індекс Кроуна-Кріспа був вищим у хворих на субклінічний гіпотиреоз (42,0±3,8; р=0,005). Після призначення замісної терапії L-тироксином ці порушення зникли.
I. Baldini і співавт. зафіксували у хворих на субклінічний гіпотиреоз погіршання логічної пам'яті (порівняно з хворими на еутиреоїдний зоб) і не виявили в них афективних порушень.
Гіпотиреоз часто призводить до вторинної гіперпролактинемії. Поєднання первинного гіпотиреозу з гіперпролактинемічним гіпогонадизмом в літературі описано під назвою «синдром Ван Віка-Росса-Геннеса». Класичне пояснення феномену гіперпролактинемії при первинному гіпотиреозі полягає в тому, що знижений рівень тиреоїдних гормонів спричинює за принципом зворотного зв'язку гіперпродукцію ТРГ, що призводить до підвищення секреції не лише ТТГ, але й пролактину. За даними різних авторів, частота розвитку гіперпролактинемії при первинному гіпотиреозі перебуває в межах 25-88%.
На думку деяких авторів, досить часто єдиним клінічним проявом гіпотиреозу є порушення ритму й провідності, що нерідко «резистентні» до антиаритмічної терапії.
Л.А. Панченкова і співавт. оцінювали стан серцево-судинної системи у хворих на ішемічну хворобу серця (ІХС) із субклінічним гіпотиреозом та еутиреозом. При цьому відзначено більшу кількість епізодів горизонтальної й максимальної глибини депресії сегмента SТ протягом доби у хворих на ІХС зі субклінічним гіпотиреозом порівняно з пацієнтами з еутиреозом (15,3 проти 2,6 і 1,16 проти 0,43 відповідно). Крім того, в групі хворих на ІХС у поєднанні зі субклінічним гіпотиреозом було виявлено ознаки безбольової ішемії міокарда в 50% випадків та істотне підвищення показників діастолічного артеріального тиску.
Біохімічне дослідження крові дає змогу виявити в пацієнтів із субклінічним гіпотиреозом порівняно зі здоровими особами знижений рівень ліпопротеїдів високої щільності (ЛПВЩ), підвищені рівні ЛПНЩ, тригліцеридів, загального холестерину, збільшений індекс атерогенності.
За даними A. Kung і співавт., порушення ліпідного обміну спостерігаються в 50% хворих на субклінічний гіпотиреоз порівняно з 20,8% у контрольній групі (підвищені рівні аполіпопротеїну А1 та В, а також співвідношення рівня загального холестерину до рівня холестерину ЛПВЩ і рівнів ЛПНЩ- і ЛПВЩ-холестерину, рівень ТТГ корелював із співвідношенням рівнів загального холестерину і ЛПВЩ-холестерину). Це дослідження підтверджує несприятливий вплив тиреоїдної недостатності на ліпідний обмін, що підвищує ризик розвитку атеросклерозу.
В.Л. Воронцов і співавт. виявили підвищений рівень ТТГ у 12,56% пацієнтів, які страждають на гіперліпідемію. А. Gupta і R.Sinha встановили підвищений рівень холестерину в пацієнтів зі субклінічним гіпотиреозом порівняно зі здоровими особами (192,13±47,40 і 157,61±37,69 мг/дл відповідно).
За даними D. Pallas і співавт., тест на антитиреоїдні антитіла був позитивним у 22 (25%) з 87 осіб із гіперхолестеринемією порівняно з 5 (6%) у контрольній групі. Крім того, у 8 осіб із гіперхолестеринемією було вперше встановлено субклінічний гіпотиреоз. У пацієнтів зі гіперхолестеринемією рівень ТТГ у середньому був вищим, ніж у контрольній групі, навіть після виключення осіб із підвищеними титрами антитиреоїдних антитіл. Було виявлено позитивну кореляцію між рівнями холестерину й ТТГ.
В.Л. Воронцов і О.И. Смирнова відзначають високий ризик розвитку атеросклерозу при гіпотиреозі в осіб віком 50 років і більше, причому в чоловіків він був вищим, ніж у жінок.
Гіперхолестеринемія при субклінічному гіпотиреозі не піддається лікуванню дієтою, статинами та іншими гіполіпідемічними препаратами, однак при цьому ефективно коригується призначенням препаратів тиреоїдних гормонів.
Крім змін ліпідного обміну, при субклінічному гіпотиреозі виявлено зниження рівня ендотеліальної вазодилатації як маркера раннього атеросклерозу. J. Lekakis і співавт. встановили негативну кореляцію між ендотелійзалежною вазодилатацією і рівнем ТТГ. Вазодилатація була найвищою в осіб із рівнем ТТГ у межах 0,4-2,0 мМО/л, нижчою – при рівні ТТГ від 2,01 до 4,0 мМО/л, ще нижчою – у пацієнтів із субклінічним гіпотиреозом і рівнем ТТГ 4,0-10,0 мМО/л і найнижчою – у пацієнтів із рівнем ТТГ понад 10,0 мМО/л.
Деякі автори знаходять зв'язок між субклінічним гіпотиреозом та ІХС у чоловіків і жінок похилого віку, однак дані S. Miura і співавт. спростовують наявність зв'язку між субклінічним гіпотиреозом, порушенням ліпідного обміну та ІХС. Обстеження 97 хворих на ІХС не виявило відмінностей за рівнем ліпідів між хворими на субклінічний гіпотиреоз і хворими з нормальною тиреоїдною функцією. Хоча в жінок із ІХС рівень тиреоїдних гормонів і ЛПВЩ-холестерину був вірогідно нижчим, автори не встановили впливу субклінічного гіпотиреозу на розвиток ІХС. Якщо хворому на ІХС показана коронарна ангіопластика, супутній субклінічний гіпотиреоз не вважається протипоказанням, оскільки не впливає на результат операції.
Дані літератури підтверджують зв'язок між субклінічним гіпотиреозом і психічними порушеннями.
R. Joffe і А. Levitt обстежували 139 пацієнтів із уніполярною депресією. У 19 з них було діагностовано субклінічний гіпотиреоз. Автори дійшли висновку, що депресія при субклінічному гіпотиреозі відрізняється від депресії в осіб без цієї патології наявністю відчуття паніки й резистентністю до лікування антидепресантами. Дослідження R. Howland підтверджує зв'язок між гіпотиреозом і рефрактерною до лікування депресією. У 52% пацієнтів із депресією, рефрактерною до лікування, було діагностовано субклінічний гіпотиреоз.
R. Kraus і співавт. обстежували хворих на депресією із рівнем ТТГ від середньої величини норми до верхньої її межі. Під час проби з ТРГ реакція ТТГ виявилася підвищеною (дельта ТТГ – понад 25 мМО/л) у 38% хворих на депресію, тому автори дійшли висновку, що субклінічний гіпотиреоз може впливати на розвиток депресії у частини хворих із вищезазначеним базальним ТТГ. Однак приблизно в 25% хворих на депресію описано знижену відповідь ТТГ на ТРГ: дельта ТТГ виявилася меншою 5 мМО/л, але все ж і не такою низькою, як при гіпертиреозі (в останньому випадку – менше 1 мМО/л). Отже, дані тиреоїдних функціональних тестів при депресивних розладах не мають односпрямованого характеру. Можна вважати, що відмінність результатів значною мірою залежить від неоднорідності груп хворих і лікування різними психотропними препаратами. На думку більшості авторів, субклінічний гіпотиреоз не можна вважати причиною розвитку депресії, але він може знижувати поріг для розвитку головних депресивних порушень.
При субклінічному гіпотиреозі відзначається зниження пізнавальної функції, погіршуються пам'ять і увага, явно або приховано знижується інтелект.
F. Моnzani і співавт. у своїх роботах оцінювали нейропсихологічні й поведінкові особливості у хворих на субклінічний гіпотиреоз та в контрольній групі. Під час оцінки за шкалою Векслера автори виявили зниження пам'яті (МQ=89,1±2,9; р=0,002) у пацієнтів зі субклінічним гіпотиреозом. Визначення індексу Кроуна-Кріспа показало незначне розходження за шкалами істерії (р=0,03), занепок
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Терапия препаратами тиреоидальных гормонов (укр)
Терапия препаратами тиреоидальных гормонов (укр)
 Клинические рекомендации Американской тиреоидологической ассоциации по диагностике и лечению узлового зоба
Клинические рекомендации Американской тиреоидологической ассоциации по диагностике и лечению узлового зоба
 К вопросу лабораторной диагностики аутоиммунных заболеваний щитовидной железы
К вопросу лабораторной диагностики аутоиммунных заболеваний щитовидной железы
 Соматотропная недостаточность: возможности современной педиатрии
Соматотропная недостаточность: возможности современной педиатрии