- Головна
- /
- Статті
- /
- Кардіологія
- /
- Пароксизмальные суправентрикулярные тахикардии: диагностика и лечение
Пароксизмальные суправентрикулярные тахикардии: диагностика и лечение
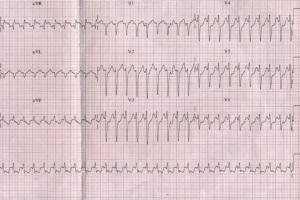
Пароксизмальные нарушения сердечного ритма – одна из наиболее острых проблем современной кардиологии. По данным Американской ассоциации кардиологов, эти нарушения ежегодно становятся причиной смерти 300-600 тыс. человек – то есть одной смерти каждую минуту, и что самое печальное, большинство этих больных – лица трудоспособного возраста.
 В последние десятилетия произошли значительные изменения в понимании клиницистами того факта, что аритмия может служить предвестником внезапной сердечной смерти (ВСС). В то же время симптомы аритмии, не являясь жизнеугрожающими, отрицательно влияют на качество жизни пациента, а в ряде случаев аритмия может оказывать влияние на ближайший и отдаленный прогнозы. Как правило, к фатальному исходу в виде остановки кровообращения приводят желудочковая фибрилляция (75% случаев), асистолия (20%) и электромеханическая диссоциация (5%), причем процент выживших пациентов, перенесших хотя бы один эпизод вышеперечисленных ситуаций, составляет 19%. C другой стороны, относительно благоприятное течение пароксизмальных нарушений сердечного ритма может осложнять множество заболеваний. Электрофизиологические механизмы тахиаритмий являются результатом сложных взаимоотношений аритмогенного субстрата и динамических модулирующих или пусковых факторов, таких как изменения гуморальной регуляции, электролитные нарушения, колебания объема циркулирующей крови, ишемия, механическое растяжение миокарда, лекарственные воздействия. Как аритмогенный субстрат, так и пусковой фактор находятся под непосредственным влиянием вегетативной нервной регуляции. Для понимания механизмов возникновения и поддержания тахиаритмии необходимо учитывать взаимодействие всех указанных трех факторов. Существует мнение о более благоприятном клиническом течении и исходах наджелудочковых тахикардий по сравнению с желудочковыми. Суправентрикулярные тахикардии (СВТ) реже ассоциируются с органическими заболеваниями сердца и дисфункцией левого желудочка, однако высокая симптоматичность, приводящая к инвалидности пациента, наличие таких опасных клинических проявлений, как пресинкопе и синкопе, внезапная аритмическая смерть (2-5%) позволяют рассматривать СВТ, как потенциально жизнеугрожающие.
В последние десятилетия произошли значительные изменения в понимании клиницистами того факта, что аритмия может служить предвестником внезапной сердечной смерти (ВСС). В то же время симптомы аритмии, не являясь жизнеугрожающими, отрицательно влияют на качество жизни пациента, а в ряде случаев аритмия может оказывать влияние на ближайший и отдаленный прогнозы. Как правило, к фатальному исходу в виде остановки кровообращения приводят желудочковая фибрилляция (75% случаев), асистолия (20%) и электромеханическая диссоциация (5%), причем процент выживших пациентов, перенесших хотя бы один эпизод вышеперечисленных ситуаций, составляет 19%. C другой стороны, относительно благоприятное течение пароксизмальных нарушений сердечного ритма может осложнять множество заболеваний. Электрофизиологические механизмы тахиаритмий являются результатом сложных взаимоотношений аритмогенного субстрата и динамических модулирующих или пусковых факторов, таких как изменения гуморальной регуляции, электролитные нарушения, колебания объема циркулирующей крови, ишемия, механическое растяжение миокарда, лекарственные воздействия. Как аритмогенный субстрат, так и пусковой фактор находятся под непосредственным влиянием вегетативной нервной регуляции. Для понимания механизмов возникновения и поддержания тахиаритмии необходимо учитывать взаимодействие всех указанных трех факторов. Существует мнение о более благоприятном клиническом течении и исходах наджелудочковых тахикардий по сравнению с желудочковыми. Суправентрикулярные тахикардии (СВТ) реже ассоциируются с органическими заболеваниями сердца и дисфункцией левого желудочка, однако высокая симптоматичность, приводящая к инвалидности пациента, наличие таких опасных клинических проявлений, как пресинкопе и синкопе, внезапная аритмическая смерть (2-5%) позволяют рассматривать СВТ, как потенциально жизнеугрожающие.
Пароксизмальные СВТ имеют следующие электрофизиологические характеристики:
- внезапные начало и окончание приступа;
- обычно регулярный ритм с небольшими колебаниями частоты;
- частота сокращений сердца от 100 до 250 уд/мин (обычно 140-220 уд/мин);
- частота сокращений желудочков соответствует частоте сокращений предсердий или меньше при наличии АВ-блокады;
- комплексы QRS, как правило, узкие, но при абберантном проведении могут расширяться.
Механизмы развития пароксизмальных аритмий и критерии диагностики
Основные механизмы развития пароксизмальных аритмий включают ри-ентри (re-entry), эктопический автоматизм и триггерную активность.
Ри-ентри, или «повторный вход» волны возбуждения – наиболее частый механизм возникновения пароксизмальных нарушений сердечного ритма, который обусловлен круговым движением волны возбуждения в миокарде и волокнах проводящей системы сердца. Для развития ри-ентри необходимы четыре условия: наличие, как минимум, двух путей проведения, односторонней блокады в одном из них, замедление проведения по другому пути и ретроградный возврат возбуждения по ранее блокированному пути к точке деполяризации. Круг ри-ентри может возникать как при наличии анатомической основы (дополнительные пути проведения, АВ-диссоциация – макрори-ентри), так и функциональной гетерогенности миокарда (микрори-ентри).
Эктопический автоматизм – это нормальное свойство клеток специализированной проводящей системы сердца. Такой способностью осуществлять во время диастолы спонтанную деполяризацию обладают клетки синусового узла (СУ), что определяет максимальную частоту генерируемых им импульсов, вследствие чего этот узел выполняет роль доминирующего водителя ритма сердца. Пароксизмальные наджелудочковые аритмии могут быть обусловлены усилением диастолической деполяризации в эктопических фокусах, расположенных в сократительном миокарде предсердий или в волокнах его проводящей системы, а также в пределах АВ-соединения. Эктопическая фокусная тахикардия становится нередко причиной непароксизмальной наджелудочковой тахикардии, один из признаков которой состоит в том, что ее начало не зависит от задержки проведения, и она может начаться в любой момент предсердного диастолического цикла, а морфология зубца Р меняется в зависимости от места нахождения очага возбуждения в предсердиях.
При определенных патологических состояниях, вызывающих уменьшение потенциала покоя, клетки проводящей системы сердца и миокарда также приобретают способность к автоматической активности, обусловленной иным механизмом – так называемыми следовыми потенциалами, которые приводят к однократному или повторяющемуся возбуждению клетки в ответ на предшествующую деполяризацию. Такой вид активности называют триггерной. Она может проявляться в различных отделах проводящей системы сердца и служить механизмом возникновения пароксизмальных наджелудочковых аритмий. Триггерная активность отличается от эктопического автоматизма тем, что спонтанная фаза деполяризации отсутствует, и очаг автоматизма начинает функционировать только после преждевременного сокращения. Предполагается, что некоторые виды аритмий, возникающие при передозировке гликозидов, – результат именно триггерной активности. Постпотенциалы могут быть усилены после введения катехоламинов или частой стимуляции миокарда. Соли калия, уменьшая амплитуду следовых потенциалов, оказывают терапевтическое воздействие.
В кардиологической практике наиболее часто встречаются следующие клинические формы пароксизмальных суправентрикулярных тахиаритмий:
- синоатриальная тахикардия;
- предсердная тахикардия;
- атриовентрикулярная узловая тахикардия;
- атриовентрикулярная реципрокная тахикардия с участием дополнительных путей проведения (при синдроме преждевременного возбуждения желудочка).
В перечисленные формы не включена синусовая тахикардия, поскольку она, являясь и физиологичной, и во многих случаях проявлением патологий (тиреотоксикоз, анемия, сердечная недостаточность и др.), никогда не носит характера пароксизмальной.
Синоатриальная (СА) тахикардия развивается по механизму ри-ентри с циркуляцией волны возбуждения в синоатриальной зоне (синусовый узел, миокард правого предсердия).
Критериями СА тахикардии являются:
- внезапное начало и прекращение;
- правильный ритм с ЧСС 100-200 уд/мин;
- зубец Р на ЭКГ практически не отличается от синусового Р.
Предсердная тахикардия – это нарушение ритма, возникающее по механизму эктопического автоматизма. К ЭКГ-критериям относят:
- правильный ритм с частотой сокращения предсердий 150-250 уд/мин;
- зубцы Р по конфигурации отличаются от синусовых;
- начало тахикардии характеризуется в ряде случаев постепенным учащением ритма, наибольшее клиническое значение имеют АВ-узловые реципрокные тахикардии.
Электрофизиологической основой пароксизмальной АВ-узловой тахикардии является наличие внутри узла двух путей проведения, обладающих различными функциональными свойствами. Один из этих путей (быстрый) проводит импульсы от предсердий к желудочкам с большей скоростью и имеет большую продолжительность эффективного рефрактерного периода. Другой путь (медленный) проводит импульс с меньшей скоростью и имеет меньшую продолжительность эффективного рефрактерного периода. Эти два пути замыкают кольцо циркуляции волны возбуждения. При нормальном синусовом ритме импульс обычно проводится через быстрый путь, поэтому функционирование медленного пути АВ-узла на ЭКГ не проявляется. При возникновении пароксизмальной АВ-узловой тахикардии импульс проводится по медленному пути к желудочкам и возвращается к предсердиям по быстрому пути. В связи с тем, что возбуждение желудочков и предсердий во время пароксизма тахикардии наступает почти одновременно, на ЭКГ редко удается зарегистрировать зубцы Р. Они, как правило, сливаются с желудочковыми комплексами. Если зубцы Р все же удается определить, то они отрицательны во II, III и aVF отведениях, что указывает на ретроградное возбуждение предсердий.
Пароксизмальная АВ-реципрокная тахикардия с участием дополнительных путей проведения (ДПП) возникает на фоне синдромов преэкситации и рассматривается в аритмологии как классическая естественная модель тахикардии, протекающей по электрофизиологическому механизму ри-ентри. Синдром преэкситации заключается в том, что во время одного сердечного цикла желудочки возбуждаются как импульсом, проведенным из предсердий по дополнительному (аномальному) пути, так и по нормально функционирующей проводящей системе, причем при проведении импульса по ДПП часть миокарда или весь желудочек возбуждается раньше, то есть преждевременно. ЭКГ-проявления синдрома преэкситации на фоне синусового ритма широко варьируют, что зависит от степени преэкситации и постоянства проведения по ДПП. Возможны следующие варианты:
- на ЭКГ постоянно имеются признаки преэкситации (манифестный синдром преэкситации);
- на ЭКГ признаки преэкситации имеют преходящий характер (интермиттирующий или преходящий синдромы преэкситации);
- ЭКГ в обычных условиях нормальная, признаки преэкситации появляются только в период пароксизма или при провокационных пробах – нагрузке, вагусных или медикаментозных пробах, электрофизиологическом исследовании (скрытый синдром преэкситации).
ЭКГ-регистрация пароксизма тахикардии является одним из важнейших условий верификации синдрома преэкситации и правильного выбора лечения. В то же время кардиологам нередко приходится сталкиваться с клиническими случаями заболевания, когда ЭКГ-регистрация пароксизма тахикардии затруднена по тем или иным причинам. В такой ситуации объективную информацию можно получить с помощью электрофизиологического исследования (ЭФИ) как неинвазивного (чреспищеводная электрокардиостимуляция – ЧПЭКС), так и инвазивного (эндокавитарное ЭФИ).
Особенно часто встречается вариант АВ-реципрокной тахикардии, при которой волна возбуждения распространяется антероградно через АВ-узел в систему Гиса-Пуркинье, ретроградно – через ДПП к предсердию. Такую тахикардию называют ортодромной. Значительно реже наблюдается вариант АВ-реципрокной тахикардии, при котором волна возбуждения совершает круговое движение по той же петле: антероградно через ДПП, ретроградно через систему Гиса-Пуркинье и АВ-узел к предсердию. Эта тахикардия получила название антидромной.
Пароксизм ортодромной СВТ характеризуется частыми (140-250 уд/мин), лишенными признаков преэкситации нормальными (узкими) комплексами QRS. В ряде случаев после комплекса QRS наблюдаются инвертированные зубцы Р, что указывает на ретроградную активацию предсердий.
Антидромная СВТ проявляется на ЭКГ частым регулярным ритмом (150-200 уд/мин), желудочковыми комплексами по типу максимально выраженной преэкситации (QRS > 0,1 с), после которых иногда выявляются инвертированные зубцы Р.
Для уточнения диагноза пароксизмальной АВ-узловой тахикардии, как правило, требуется клиническое электрофизиологическое исследование. Пароксизмальная наджелудочковая тахикардия при скрытом синдроме WPW имеет определенное сходство с АВ-узловой тахикардией, но отличается структурой цепи ри-ентри, поэтому дифференциальная диагностика между ними строится на признаках, выявляющих участие различных структур в цепи ри-ентри.
Наиболее полезная информация при дифференциации АВ-узловой и реципрокной тахикардии с участием ДПП может быть получена на чреспищеводной электрограмме при пароксизме тахикардии. Величина интервала VА, по данным пищеводного отведения менее 100 мс, в 90% случаев указывает на АВ-узловую тахикардию. При этом зубец Р на наружной ЭКГ не виден, так как он накладывается на комплекс QRS или начало сегмента ST.
Сегодня существует Европейский стандарт для диагностики и лечения аритмий. При подозрении на аритмию врач должен установить факт нарушений ритма, определить аритмию, ее причину, функциональный или патологический характер и решить вопрос о применении антиаритмической терапии. Для этих целей используют физикальные исследования, ЭКГ, суточный ЭКГ-мониторинг (по Холтеру), пищеводную электрокардиографию.
Учитывая сложности диагностики пароксизмальных нарушений ритма согласно международным рекомендациям все тахиаритмии разделяются на два типа.
- Тахикардия с узким комплексом QRS (антеградное проведение через AV-узел); наиболее часто – это суправентрикулярная пароксизмальная тахикардия; ее купируют осторожно, внутривенно вводят верапамил, пропранолол или дигоксин.
- Тахикардия с широким комплексом QRS (антеградное проведение через дополнительный путь) часто сочетается с фибрилляцией предсердий и очень высокой (>250 уд/мин) частотой сокращений желудочков; при нестабильных гемодинамических показателях показана немедленная кардиоверсия; медикаментозное лечение проводят лидокаином или прокаинамидом внутривенно.
Аритмии с узким комплексом QRS:
- синусовая тахикардия – ЧСС 100-160 (уд/мин) при нормальном зубце Р;
- пароксизмальная суправентрикулярная тахикардия – при ЧСС 140-250 (уд/мин), зубец Р заострен или инвертирован в отведениях II, III, aVF;
- трепетание предсердий – ЧСС 250-350 (уд/мин), волны трепетания в виде «зуба пилы», с блокадой проведения на желудочки 2:1, 4:1;
- фибрилляция предсердий – ЧСС > 350 (уд/мин), зубец Р неразличим, промежутки QRS нерегулярные;
- многофокусная предсердная тахикардия – при ЧСС 100-220 (уд/мин), более чем три дифференцированные формы зубца Р с различными интервалами Р-Р.
Аритмии с широким комплексом QRS:
- желудочковая тахикардия – умеренно выраженная нерегулярность при ЧСС 100-250 (уд/мин);
- желудочковая тахикардия типа «пируэт»;
- фибрилляция желудочков;
- суправентрикулярные тахикардии с аберрантной вентрикулярной проводимостью – широкий комплекс QRS с типичным для суправентрикулярного ритма зубцом Р.
При широких комплексах QRS (более 120 мс) важно дифференцировать наджелудочковые тахикардии от желудочковой тахикардии (ЖT). Если диагноз НЖТ невозможно подтвердить или установить, то тахиаритмию следует расценивать как ЖT и соответственно лечить. Тахикардия с широкими комплексами QRS может быть разделена на три группы:
- СВТ с блокадой ножек пучка Гиса;
- СВТ c проведением по дополнительному предсердно-желудочковому соединению (ДПЖС);
- желудочковая тахикардия.
Суправентрикулярная тахикардия с блокадой ножек пучка Гиса. Блокада ножек пучка Гиса (БНПГ) может выявляться исходно или возникать только во время тахикардии, когда одна из ветвей пучка Гиса находится в рефрактерном периоде из-за частого ритма. Возникновение большинства БНПГ зависит не только от частоты ритма, но также от последовательности интервалов R-R – «длинный-короткий». Блокада ножек пучка Гиса может возникнуть при любой НЖТ. Если во время ортодромной АВРТ развивается БНПГ, то частота тахикардии может уменьшиться, если блокированная ножка пучка Гиса расположена на той же стороне (ипсилатеральная блокада), что и ДПЖС.
Суправентрикулярная тахикардия с проведением по ДПЖС. СПТ с участием ДПЖС возникает во время ПТ, трепетания предсердий, ФП, АВУРТ или антидромной АВРТ. Последняя развивается при антероградном проведении по ДПЖС и ретроградном проведении по атриовентрикулярному узлу или второму ДПЖС. Широкий комплекс QRS с морфологией блокады левой ножки пучка Гиса (БЛНПГ) наблюдается при антероградном проведении по другим видам дополнительных путей, таким как атриофасцикулярный, нодофасцикулярный или нодовентрикулярный.
<i>Желудочковая тахикардия. Существуют ЭКГ-критерии, которые позволяют дифференцировать основной механизм тахикардии с широким комплексом QRS. Тахикардии с широкими комплексами QRS >120 мс у взрослых могут быть вызваны наджелудочковыми аритмиями с постоянным или частотнозависимым аберрантным внутрижелудочковым проведением, наджелудочковыми аритмиями с антеградным предвозбуждением, а также желудочковыми аритмиями. Несмотря на предложенные многими авторами ЭКГ-критерии для дифференцирования наджелудочковой тахикардии с аберрантным проведением и желудочковой тахикардией, эти различия могут вызывать затруднения, даже если для анализа доступны полные записи ЭКГ. Аритмии с антеградным предвозбуждением вызывают особые трудности при дифференцировке с ЖТ на основании только морфологических критериев комплексов QRS. При некоторых аритмиях, таких как re-entry с вовлечением ветвей пучка Гиса или тахикардии при наличии атриофасцикулярных трактов (АФТ), конфигурация QRS не отличается от более распространенных форм наджелудочковых тахикардий с аберрантным проведением. Наконец, некоторые виды ЖТ могут иметь комплексы QRS продолжительностью 120 мс при аномальной морфологии QRS, у детей продолжительность комплексов QRS при ЖТ составляет нередко менее 120 мс. Электрофизиологическое исследование позволяет точно диагностировать практически все тахикардии с широкими комплексами, а также определить последовательность и взаимоотношения между активацией предсердий и желудочков. При этом можно зарегистрировать электрограммы от структур, не отражающихся на стандартной ЭКГ, (таких как пучок Гиса или дополнительные пути проведения), а также проанализировать ответы на различные пробы со стимуляцией. Поскольку знание механизма аритмии обычно имеет критическое значение для выбора надлежащей терапии, электрофизиологические исследования часто занимают важное место в клинической диагностике у пациентов, имеющих тахикардии с широкими комплексами.
Лечение аритмий
Лечение аритмий сердца – один из наиболее противоречивых вопросов кардиологии. Известно, что многие расстройства сердечного ритма оказывают серьезное негативное влияние на качество жизни, имеют неблагоприятное прогностическое значение и поэтому требуют лечения. С другой стороны, в ряде рандомизированных многоцентровых исследований (Coplen, CAST-1, CAST-11 и др.) показано, что длительный прием антиаритмических препаратов, относящихся к 1 классу по классификации Vaughan Williams, может неблагоприятно влиять на жизненный прогноз. В связи с этим представляется очевидным, что целью антиаритмической терапии должно быть не только и не столько устранение самой аритмии, сколько улучшение качества жизни больного с гарантией безопасности этого лечения.
Определение тактики лечения аритмий
При обследовании пациента с каким-либо нарушением сердечного ритма или проводимости необходимо в первую очередь разобраться в характере аритмии, определить ее клиническое значение и установить, нуждается ли больной в специальной антиаритмической терапии. При выявлении безопасной аритмии в отсутствие органического заболевания сердца врачу не следует фиксировать внимание пациента на обнаруженных изменениях. Нужно объяснить, что аритмия ничем ему не угрожает и не требует специального лечения. В некоторых случаях больного, который очень обеспокоен наличием у него аритмий, убедить в этом не удается. Тогда приходится назначать симптоматическую терапию (седативные, метаболические, общеукрепляющие препараты).
Определяя тактику лечения аритмий, следует в первую очередь попытаться установить их этиологию, то есть заболевание, лежащее в их основе. Иногда этиологическая терапия сама по себе достаточна для устранения аритмии без использования специальных антиаритмических средств, применение которых без воздействия на основное заболевание нередко малоэффективно. Это касается, в частности, нарушений ритма у больных тиреотоксикозом, ревмокардитом, миокардитами различной этиологии, острыми формами ИБС и некоторыми другими заболеваниями. При хронических заболеваниях сердца этиологическая терапия во многих случаях невозможна или неэффективна. Однако при внимательном обследовании больного можно выявить патогенетические факторы и условия, способствующие развитию аритмии: психоэмоциональные реакции, симпатические или парасимпатические влияния, аритмогенное действие медикаментозных препаратов, нарушения электролитного баланса, метаболический ацидоз и другие. Их устранение и терапевтическое воздействие играют важную роль в успешном лечении больных. После оценки этиологических и патогенетических факторов легче выбирать среди многочисленных средств и методов антиаритмической терапии те, которые показаны данному пациенту.
Выбор антиаритмического препарата в значительной степени зависит от формы аритмий, так как многие антиаритмические средства влияют избирательно или преимущественно на конкретные формы расстройства ритма.
Необходимо также учитывать индивидуальную чувствительность больного к тому или иному препарату. При расспросе пациента следует обратить особое внимание на эффективность ранее применяемых антиаритмических средств и их переносимость, учесть психологическую настроенность больного на прием того или иного средства, веру в его эффективность или, наоборот, негативное к нему отношение. Если больной ранее не получал препарата, который врач предполагает ему назначить, но есть основания опасаться побочных действий, целесообразно начать лечение с небольших пробных доз и, лишь удостоверившись в хорошей переносимости, применять терапевтические дозы.
Назначая медикаментозную антиаритмическую терапию, очень важно правильно подобрать дозу препарата, причем желательно минимальные эффективные дозы. При отсутствии эффекта препарата, назначаемого в средних терапевтических дозах, предпочтительнее не наращивать их до максимальных (это значительно повысит вероятность побочных действий), а подобрать другой препарат или комбинацию препаратов.
Комбинирование антиаритмических препаратов – еще недостаточно изученный аспект проблемы лечения аритмий. Известно, что при сочетании некоторых антиаритмических препаратов происходит взаимопотенцирование терапевтического действия. Целесообразнее сочетать препараты с различными механизмами действия, относящиеся к разным классам, в частности – препараты I и II классов, β-адреноблокаторы с амиодароном или с препаратами дигиталиса.
Особое место занимает соталол – единственный препарат, объединяющий свойства антиаритмических средств II и III классов (сочетает свойства β-адреноблокатора и блокатора калиевых каналов). Он обладает хорошим фармакологическим профилем (начало действия наступает через 1 час после перорального приема, не меняет фармакодинамики других препаратов при комбинированной терапии, не кумулирует в тканях организма), характиризуется низким уровнем побочных эффектов, а также является препаратом выбора для лечения пациентов с нарушениями сердечного ритма в сочетании с АГ и ИБС. Клинический опыт применения соталола насчитывает более полутора тысяч исследований.
Нецелесообразно комбинировать препараты, взаимоусиливающие нежелательные действия, например препараты дигиталиса с хинидином, амиодароном и верапамилом, так как при этих сочетаниях повышается концентрация дигиталиса в крови. Применение β-адреноблокаторов в сочетании с верапамилом может привести к резкому угнетению синусового автоматизма и нарушению атриовентрикулярной проводимости, а также к снижению сократительности миокарда. Опасно сочетание препаратов классов IА и III из-за риска развития синдрома удлиненного QT, нерационально комбинирование препаратов класса IC из-за опасности нарушения проводимости и аритмогенного действия.
Индивидуальный подбор эффективных антиаритмических препаратов (ААП) следует проводить в острой пробе во время ЭФИ (серийное тестирование ААП). Отмечается высокая корреляция между результатами острого тестирования и эффективностью ААП при их последующем длительном приеме. Выбор оптимального ААП зависит от механизма тахиаритмии, сопутствующих заболеваний, провоцирующих факторов, электрофизиологических свойств проводящей системы сердца и ДПП. Способ купирования пароксизма тахикардии определяется в зависимости от его тяжести, которая связана с частотой сердечных сокращений, состоянием гемодинамики и длительностью приступа.
Неотложная терапия тахикардии с узкими комплексами QRS
Для купирования тахикардии с узкими комплексами QRS следует начинать с вагусных приемов (проба Вальсальвы, массаж каротидного синуса, погружение лица в холодную воду и т. д.), влияющих на AВ-проводимость. При отсутствии положительного эффекта пациентам со стабильной гемодинамикой начинают внутривенное введение противоаритмических препаратов. Препаратами выбора являются аденозин (АТФ) или антагонисты кальциевых каналов негидропиридинового ряда. Преимущества аденозина, по сравнению с блокаторами кальциевых каналов или β-адреноблокаторами при внутривенном введении, состоит в быстром начале действия и коротком периоде полувыведения, поэтому чаще всего предпочтение отдают внутривенному введению аденозина, за исключением пациентов с тяжелой бронхиальной астмой. Препараты длительного действия (блокаторы кальциевых каналов или β-адреноблокаторы) используют у пациентов с частыми предсердными или желудочковыми экстрасистолами, которые становятся пусковым механизмом непароксизмальных НЖТ. Аденозин или электроимпульсная терапия (кардиоверсия) являются методом выбора у лиц с гемодинамически значимой НЖТ. Аденозин провоцирует фибрилляцию предсердий в 1-15% случаев, которая обычно носит временный характер, но может быть жизнеугрожающей у пациентов с синдромом предвозбуждения желудочков. Необходимо соблюдать крайнюю осторожность при одновременном внутривенном назначении блокаторов кальциевых каналов и β-адреноблокаторов, поскольку существует опасность возникновения гипотензии и/или брадикардии. Во время выполнения вагусных приемов или введения препаратов целесообразна регистрация ЭКГ, поскольку реакция на них может помочь в диагностике, даже если аритмия не прекратилась. Купирование тахикардии с зубцом Р, расположенным после комплекса QRS, предполагает диагноз АВРТ или АВУРТ. Предсердная тахикардия часто нечувствительна к аденозину. Трансформация в тахикардию с AВ-блокадой фактически указывает на ПТ или трепетание предсердий (в зависимости от интервала P-P или F-F), исключает AВРT и делает AВУРT маловероятной.
Лечение тахикардий с широкими комплексами QRS
Экстренная электроимпульсная терапия показана при гемодинамически значимых тахикардиях. Если тахикардия не приводит к гемодинамическим нарушениям и является наджелудочковой, то лечение ее такое же, что и тахикардии с узкими комплексами QRS. Для купирования тахикардии с широкими QRS комплексами при отсутствии нарушений гемодинамики можно использовать парентеральные формы прокаинамида и/или соталола (рекомендации даны на основании малочисленных рандомизированных исследований). Также может быть использован амиодарон, ему отдают предпочтение, по сравнению с прокаинамидом и соталолом, при лечении пациентов со сниженной фракцией выброса левого желудочка или с признаками сердечной недостаточности. В отдельных случаях требуется альтернативная терапия, например, при тахикардии с предвозбуждением желудочков и желудочковой тахикардии при дигиталисной интоксикации. Для купирования неритмичной тахикардии с широким комплексом QRS (фибрилляция предсердий с проведением по ДПЖС) рекомендуется электроимпульсная терапия. Если у пациента нет гемодинамических нарушений, можно прибегнуть к фармакологической кардиоверсии с в/в введением ибутилида или флекаинида.
После успешного купирования тахикардии с широкими комплексами QRS неизвестной этиологии пациентам следует обратиться к аритмологу. Пациентам с гемодинамичесчки незначимой тахикардией с узкими комплексами QRS, сохранной функцией левого желудочка и нормальной ЭКГ во время синусового ритма (отсутствие синдрома предвозбуждения желудочков) специфическая терапия может не потребоваться. Консультация врача-специалиста показана и тем пациентам, которые резистентны к лекарственной терапии или плохо ее переносят, а также лицам, не желающим постоянно принимать антиаритмические препараты. При необходимости лечения должен быть сделан выбор: катетерная абляция или лекарственная терапия. В связи с риском летального исхода всем больным с синдромом WPW (синдром предвозбуждения желудочков в сочетании с аритмией) показано дальнейшее обследование.
Последовательность введения антиаритмических препаратов при различных видах СВТ изложена в таблице.
Лечение синусовой тахикардии заключается в терапии основного заболевания. При вегетативной дисфункции показаны физические тренировки, особенно упражнения циклического характера: ходьба, легкий бег, плавание, лыжи, велосипед. Из медикаментозных средств обычно используют β-блокаторы, под влиянием которых нередко уменьшаются и сопутствующие вегетативные симптомы (потливость, тремор, слабость и головокружение).
Для оказания неотложной помощи больному с пароксизмом наджелудочковой тахикардии точного определения ее механизма не требуется, прежде всего необходимо успокоить больного. Купирование пароксизма, как правило, начинают с применения вагусных проб. Самостоятельно больные могут использовать пробу Вальсальвы (сильное натуживание в течение 10-15 с после глубокого вдоха), провоцировать рвотный рефлекс путем раздражения корня языка или задней стенки глотки. Врач обычно прибегает к массажу каротидного синуса (ниже уровня угла нижней челюсти и выше щитовидного хряща в течение 5-10 с). Эту процедуру проводят больному, находящемуся в положении лежа. Более эффективен массаж правого каротидного синуса, массировать его с двух сторон одновременно нельзя. Противопоказанием к применению этой процедуры является перенесенное в прошлом нарушение мозгового кровообращения. Иногда приступы купируются при глубоком вдохе, с помощью кашля. Купирующий эффект вагусных воздействий достигает 70-80%. При неэффективности этих мероприятий переходят к медикаментозному лечению (таблица).
Необходимо подчеркнуть, что купирование антидромной тахикардии, фибрилляции предсердий на фоне синдромов преэкситации и тахикардий с широкими комплексами QRS имеет определенные особенности. В частности, не следует применять сердечные гликозиды и верапамил, дилтиазем, β-блокаторы (пропранолол, атенолол, надолол, метопролол, соталол) из-за возможности улучшения проведения по дополнительному пути и возникновения трепетания или фибрилляции желудочков.
Если тахикардию не удается купировать с помощью лекарственных препаратов и развиваются нарушения гемодинамики, проводят электроимпульсную терапию. Синусовый ритм обычно восстанавливается при использовании электрического разряда невысокой мощности.
Профилактическую терапию для больных с частыми приступами тахикардии (чаще одного раза в неделю) подбирают, последовательно назначая препараты: прекращение пароксизмов служит критерием эффективности препарата. У больных с редкими нетяжелыми хорошо переносимыми приступами нет необходимости в постоянном приеме антиаритмических препаратов, им целесообразно подобрать препарат для самостоятельного купирования приступов.
При рефрактерных к медикаментозной терапии тяжелых приступах, особенно у больных с синдромом WPW, используют хирургические методы лечения.
Фибрилляция предсердий является жизнеугрожающей у пациентов с WPW-синдромом. Если дополнительный путь имеет короткий антероградный рефракторный период, то проведение импульсов на желудочки с высокой частотой во время фибрилляции предсердий может привести к фибрилляции желудочков. Приблизительно у трети пациентов с синдромом WPW имеется ФП. ДПЖС играют патофизиологическую роль в развитии ФП у данной категории больных, большинство из них лица молодого возраста, не имеющие структурной патологии сердца. АВРТ с высокой частотой ритма может иметь определенное значение в индукции ФП. Хирургические методы лечения или катетерная абляция дополнительных путей способны устранить ФП, также как и АВРТ. Частота случаев внезапной смерти среди пациентов с синдромом WPW варьирует от 0,15 до 0,39% в течение динамического наблюдения от 3 до10 лет. Остановка сердца редко является первым проявлением синдрома WPW. В то время как при анализе остановок сердца, почти в половине случаев их причиной является WPW-синдромом. Учитывая потенциальную возможность у таких пациентов развития ФП и риск внезапной смерти в результате ФП, недопустима даже низкая частота ежегодных случаев внезапной смерти среди пациентов с синдромом WPW, имеет значение необходимость проведения катетерной абляции. Исследование пациентов с WPW-синдромом, перенесших остановку сердца, ретроспективно определило ряд критериев, с помощью которых можно выявить пациентов с повышенным риском внезапной смерти. К ним относятся:
- укороченный R-R (менее 250 мс при предвозбуждении желудочков во время спонтанной или индуцированной ФП);
- анамнез симптоматичной тахикардии;
- множественные дополнительные пути;
- аномалия Эбштейна.
Сообщалось о высокой частоте внезапной смерти при семейном синдроме WPW, хотя такая форма крайне редка. Предлагалось проведение ряда неинвазивных и инвазивных исследований, помогающих стратифицировать риск внезапной смерти. Выявление интермиттирующего синдрома предвозбуждения желудочков, характеризующегося внезапным исчезновением дельта-волны и нормализацией комплекса QRS, свидетельствует о том, что дополнительный путь имеет относительно длинный рефракторный период, и возникновение ФЖ маловероятно. Исчезновение предвозбуждения после введения противоаритмического препарата прокаинамида также использовалось для того, чтобы определить подгруппу низкого риска. Считается, что неинвазивные методы исследования уступают инвазивной электрофизиологической оценке риска внезапной смерти, поэтому в настоящее время неинвазивные методы не играют большой роли при исследовании пациентов.
Катетерная абляция у больных с синдромом WPW
Перед катетерной абляцией ДПЖС выполняют ЭФИ, цель которого подтверждение наличия дополнительного пути, определение его электрофизиологических характеристик и роли в формировании тахиаритмии. После определения локализации дополнительного пути выполняют радиочастотную абляцию (РЧА) ДПЖС с использованием управляемого абляционного катетера. К сожалению, проспективных рандомизированных клинических исследований, в которых оценивались безопасность и эффективность катетерной абляции ДПЖС, не проводилось, хотя о результатах катетерной абляции дополнительных путей сообщалось в большом количестве одноцентровых исследований, одном многоцентровом исследовании и нескольких проспективных наблюдениях. В большинстве наблюдений первичная эффективность катетерной абляции ДПЖС составляла приблизительно 95%. Эффективность при катетерной абляции ДПЖС, локализованных в боковой стенке левого желудочка, немного выше, чем при катетерной абляции дополнительных путей другой локализации. Рецидивы проведения по ДАВС возникают приблизительно в 5% случаев, что связано с уменьшением отека и воспалительных изменений, обусловленных повреждающим действием РЧ-энергии. Повторная РЧА, как правило, полностью устраняет проведение по ДПЖС.
Осложнения при проведении эндо-ЭФИ и РЧА дополнительных путей можно разделить на четыре группы:
- обусловленные лучевой нагрузкой;
- связанные с пункцией и катетеризацией сосудов (гематома, тромбоз глубоких вен, перфорация артерий, артериовенозная фистула, пневмоторакс);
- при катетерных манипуляциях
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Электрокардиография: о чем расскажет результат ЭКГ?
Электрокардиография: о чем расскажет результат ЭКГ?
 Диагностика и лечение фибрилляции предсердий
Диагностика и лечение фибрилляции предсердий
 Ведение пациентов с обморочными состояниями. Рекомендации Европейского общества кардиологов
Ведение пациентов с обморочными состояниями. Рекомендации Европейского общества кардиологов
 Конгресс «Лекарства и жизнь»
Конгресс «Лекарства и жизнь»