- Головна
- /
- Статті
- /
- Акушерство, гінекологія, репродуктивна медицина
- /
- Актуальные аспекты проведения и прекращения реанимации глубоконедоношенных детей на этапе родильного зала
Актуальные аспекты проведения и прекращения реанимации глубоконедоношенных детей на этапе родильного зала
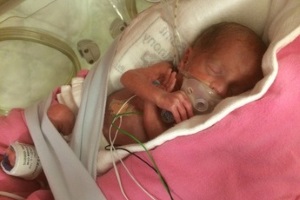
Примерно 10% всех новорожденных требуют активных реанимационных мероприятий для появления громкого крика или регулярного дыхания, поддержания частоты сердечных сокращений на уровне выше 100 уд/мин и достижения нормального цвета кожи и мышечного тонуса.
Основные принципы реанимации новорожденных (алгоритм: оценка-решение-действие) приемлемы как для доношенных, так и для недоношенных детей (J. Kattwinkel). В западной литературе термин «newly born» отражает специфику состояния ребенка в первые минуты и часы жизни, а термин «neonate» – до 28 дней (включительно). Младенчество включает неонатальный период и продолжается до конца первого года жизни. Чем меньше гестационный возраст ребенка, тем чаще возникает необходимость проведения реанимационных мероприятий в полном объеме, тем важнее прогнозирование и адекватная подготовка к родам.
Особенности подготовки к рождению глубоконедоношенных детей
Помещение
В распоряжении медперсонала должно быть чистое и теплое помещение, с полным набором реанимационного оборудования и медикаментов, с источником лучистого тепла.
Особое значение для проведения реанимации недоношенных детей имеет соблюдение «тепловой цепочки» новорожденного. Жировая клетчатка таких детей слабо выражена, соотношение площади поверхности тела и массы достаточно высоко, им сложно осуществлять полноценную терморегуляцию организма. С учетом этого желательно первичную помощь новорожденным проводить в инкубаторе открытого типа с системой сервоконтроля, в котором интенсивность обогрева ребенка строго контролируема и зависит от заданной температуры. Гипертермия способствует пренатальной дыхательной депрессии, гипотермия – развитию внутрижелудочковых кровоизлияний. При отсутствии источника лучистого тепла необходимо создать комфортную температуру во всем помещении (таблица).
Персонал
Успех проведения первичной реанимации недоношенных детей во многом зависит от персонала. Необходимо присутствие, по меньшей мере, двух человек, владеющих техникой первичной реанимации. Один – обеспечивает адекватную вентиляцию легких и/или проводит интубацию, второй – контролирует сердцебиение и проводит при необходимости непрямой массаж сердца. Действия реанимационной бригады должны осуществляться по определенным правилам, специалисты – подчиняться одному руководителю.
Когда интубировать?
Наиболее часто на практике доктор должен решить вопрос, нуждается ли недоношенный ребенок в неотложной интубации сразу после рождения? В литературе отсутствуют четкие рекомендации по данной проблеме. Ранняя интубация детей с гестационным возрастом менее 28 недель необходима, по мнению многих экспертов, для правильного формирования воздушно-жидкостного барьера, по другим источникам – рекомендуются с этой целью подача дополнительного кислорода ребенку, а затем интубация.
В пользу неотложной интубации свидетельствует то, что незрелость головного мозга и наличие хрупкого герминального матрикса у глубоконедоношенных детей предрасполагают к развитию внутричерепных кровоизлияний после эпизода гипоксии или резкого изменения давления и осмолярности крови в сосудистом русле. Сниженная податливость легочной ткани, слабость дыхательной мускулатуры приводят к тому, что глубоконедоношенный ребенок нуждается во вспомогательной искусственной вентиляции легких (ИВЛ).
Время введения препаратов сурфактанта
Учитывая, что 60% новорожденных, родившихся ранее 30-й недели гестации, и 80% новорожденных – ранее 28-й недели, имеют дефицит сурфактанта, вопрос о целесообразности начала ранней сурфактантной заместительной терапии решается одновременно с проведением стандартной первичной реанимации новорожденного. Первичную реанимацию глубоконедоношенных новорожденных необходимо рассматривать не только как восстановление жизненно важных функций организма, но и как возможность для раннего проведения заместительной сурфактантной терапии.
Заместительная терапия сурфактантом уменьшает поверхностное натяжение, стабилизирует альвеолы, позволяя альвеолярным стенкам оставаться расправленными. Введение сурфактанта разделяют на профилактическое и лечебное.
Профилактическое введение – это инстилляция сурфактанта при проведении реанимации в родильном зале сразу после интубации. При таком введении сурфактант распределяется более гомогенно, так как легкие еще наполнены фетальной жидкостью. Недостатком профилактического назначения сурфактанта является то, что если его назначить до оценки положения интубационной трубки, он может попасть в одно легкое, а также помешать проведению полноценной реанимации и дестабилизировать состояние.
Поскольку введение относительно большого объема жидкости в дыхательные пути нередко усложняет реанимацию, желательно применять сурфактанты с содержанием терапевтической дозы в небольшом объеме флакона.
Лечебное введение – это инстилляция сурфактанта новорожденному в течение нескольких часов после рождения, когда диагностирован респираторный дистресс-синдром (РДС) и ребенок находится на ИВЛ. Теоретически эпителий легких недоношенных новорожденных повреждается в пределах нескольких минут ИВЛ. Белки сыворотки могут просачиваться на поверхность альвеол и ингибировать функции сурфактанта. РДС обычно развивается в первые 6 часов после родов: появляются клинические признаки РДС (тахипноэ с частотой дыхания до 60 в 1 мин, диспноэ с преобладанием диафрагмального паттерна, раздувание крыльев носа, экспираторные хрипы и стоны, втягивание грудной клетки).
Время, потраченное в ожидании того, чтобы установить диагноз более точно, снижает эффективность терапии. Новорожденные с РДС подвержены ряду осложнений: бронхолегочной дисплазии, задержке воздуха в легких с развитием интерстициальной эмфиземы легких (ИЭЛ), попаданию воздуха в грудную клетку с развитием пневмоторакса (ПТ), бронхолегочной дисплазии (БЛД).
В последнее время в Украине проведение лечебно-диагностических мероприятий регулируется признанной концепцией доказательной медицины, как основы для разработки национальных протоколов и стандартов. В библиотеке Сochrane представлено достаточное количество материалов по использованию препаратов сурфактанта как с лечебной, так и с профилактической целью. Kendig и соавт. сравнивали эффективность введения естественного сурфактанта сразу после интубации в родильном зале и после стандартной реанимации и определения положения эндотрахеальной трубки (ЭТТ) у новорожденных сроком гестации менее 29 недель. Оба введения оказались одинаково эффективны.
Профилактическое эндотрахеальное введение естественного сурфактанта новорожденным с риском развития РДС (интубированные младенцы со сроком гестации менее 30 недель) улучшает клинический результат, при этом уменьшается риск пневмоторакса, появления ИЭЛ, БЛД и смерти (R.F. Soll, 1997).
Профилактическое эндотрахеальное введение синтетического сурфактанта младенцам с риском развития РДС улучшает клинический результат: снижается риск пневмоторакса, появления ИЭЛ и смерти, повышается частота возникновения открытого артериального (боталлового) протока (ОАП) и легочного кровоизлияния (R.F. Soll, 1998).
Ранняя заместительная терапия сурфактантом с экстубацией и назальным CPAP (Continuous Positive Airway Pressure) – вентиляция при постоянном положительном давлении в дыхательных путях), по сравнению с поздним селективным введением сурфактанта и длительной ИВЛ с экстубацией от низкой дыхательной поддержки, приводит к уменьшению необходимости в проведении ИВЛ и увеличении доз применяемого сурфактанта (T.P. Stevens, M. Blennow, R.F. Soll, 2002). Однако эти выводы основаны на результатах одного небольшого рандомизированного клинического исследования и необходимы дополнительные исследования.
Отказ от реанимации
Рождение крайне незрелых новорожденных и детей с тяжелыми врожденными пороками развития – ситуация, когда специалисты должны решить вопрос об отказе от проведения реанимационных мероприятий. Четких критериев для выработки показаний, обусловливающих отказ от реанимации, нет, существует лишь множество работ, посвященным медицинским, юридическим и этическим аспектам данной проблемы.
На данный момент приняты следующие правила. Отказ от реанимации в родовом зале допустим, если гестационный возраст новорожденного меньше 23 недель или масса при рождении менее 400 г, подтверждено наличие анэнцефалии или трисомии по 13-й или 18-й хромосомам. Современные данные говорят о том, что при проведении реанимационных мероприятий у таких детей выживание маловероятно либо ребенок остается глубоким инвалидом (класс IIb, уровень доказательности Е).
Duff и Campbell (1973) впервые признали факт отказа от реанимации по согласованию с родителями ввиду неприемлемого качества жизни или низкого шанса ребенка на выживание. Остается практически неизвестной точка зрения самих родителей, в то время как решение о прекращении интенсивной терапии является их прерогативой.
В случае неопределенного прогноза, с учетом гестационного возраста, реанимация включает пробную терапию и отказ от начала или продолжения реанимации новорожденного. В таком случае начало реанимационных мероприятий не подразумевает длительной поддержки новорожденного.
Отказ от начала реанимации и последующее ее прекращение, с этической точки зрения, равнозначны, однако последний вариант предоставляет больше времени на полную клиническую оценку и позволяет посоветоваться с семьей. Врач должен объяснить родителям оценку состояния новорожденного, последствия продолжения и прекращения реанимации. В общем, преимуществ в том, чтобы отсрочить проведение мероприятий либо проводить их частично, нет; если ребенок выживает, то результаты могут быть хуже именно вследствие этих действий.
Прекращение реанимации
Прекращение реанимационных мероприятий допустимо в случае, если полноценная реанимация ребенка при остановке дыхания и сердечной деятельности не привела к восстановлению витальных функций в течение 15 минут. Реанимация новорожденного с асистолией более 10 минут, скорее всего, не позволит сохранить жизнь новорожденного либо приведет к глубокой инвалидизации ребенка (класс IIb, уровень доказательности Е). По нашему мнению, эта проблема должна решаться на местах после обсуждения этого вопроса и создания местных инструкций в соответствии с условиями и результатами работы неонатальной службы.
Помощь семье
Если время позволяет, члены реанимационной бригады новорожденных должны представиться матери и семье, изложить план проведения реанимационных мероприятий и ответить на возникшие у родителей и/или близких вопросы. В случае, когда возможно рождение ребенка с несовместимыми с жизнью пороками или крайне недоношенного, необходимо просить родителей четко сформулировать их соображения и пожелания о продолжительности реанимации.
Нужно помнить что после родов мать сама еще остается пациентом с соответствующими физическими и эмоциональными потребностями. Бригада, работающая с новорожденным, при первой возможности должна сообщить родителям о его состоянии. Если ребенку требуется неотложная помощь, необходимо информировать родителей обо всех манипуляциях и их назначении. Специалисты должны способствовать тому, чтобы родители задавали вопросы и получали на них искренние и честные ответы. При этом необходимо использовать каждую возможность для общения родителей и новорожденного.
Выводы
Приведенные в статье данные свидетельствуют о существовании структурированного подхода к проведению реанимационных мероприятий у новорожденных детей. В настоящее время рабочая группа Ассоциации неонатологов Украины работает над созданием клинического протокола МЗ Украины «Реанимация новорожденных».
Литература
- Kattwinkel J., Добрянский Д. Реанимация новорожденных. MD, FAAP. – С. 3-16.
- Энкин М., Кейс М. и соавт. Руководство по эффективной помощи при беременности и рождении ребенка. СПБ.: Нордмед-издат, 1999. – С. 386-387.
- Актуальні питання неонатології / Матеріали ІV конгресу неонатологів України. – С. 3-5.
- Morley C. Systematic review of prophylactic vs rescue surfactant // Arch Dis Child Fetal Neonatal Ed 1997; 77: F70-F74.
- Gandy G., Jacobson W., Gairdner D. Hyaline membrane disease I cellular changes. Arch Dis Child 1970; 45: 289-310.
- Robertson B., Berry D., Curstedt T., Grossmann G., Ikegami M., Jacobs M. et al. Leakage of protein in the immature rabbit lung; effect of surfactant replacement // Respir Physiol 1985; 61: 265-276.
- Ryan R., Robert A. Sinkin, William M. Maniskalco et al. Comparison of Two Strategies for Surfactant Prophylaxis in Very Premature Infants: A Multicenter Randomized Trial // PEDIATRICS. – 1998. – Vol. 101. – Р. 1006-1012)
- Seeger W., Stohr G., Wolf H.R.D., Heuhof H. Alteration of surfactant function due to protein leakage: special interaction with fibrin monomer // J Appl Physiol 1985; 58: 326-338.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Проблема сепсиса у детей. Начало.
Проблема сепсиса у детей. Начало.
 Гастродуоденальная патология у детей: проблемы и перспективы
Гастродуоденальная патология у детей: проблемы и перспективы
 Кесарево сечение: прошлое, настоящее и будущее
Кесарево сечение: прошлое, настоящее и будущее
 Беременность и сахарный диабет
Беременность и сахарный диабет