- Головна
- /
- Статті
- /
- Інфекційні захворювання
- /
- Современные подходы к профилактике и лечению вульвовагинального кандидоза
Современные подходы к профилактике и лечению вульвовагинального кандидоза
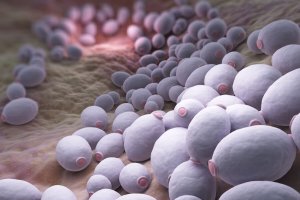
Вульвовагинальный кандидоз остается одной из важнейших проблем гинекологии, дерматовенерологии и микологии. Необычайно широкая распространенность заболевания, его устойчивость к терапии и длительное течение заставляют многих врачей обращать внимание на
Вульвовагинальный кандидоз остается одной из важнейших проблем гинекологии, дерматовенерологии и микологии. Необычайно широкая распространенность заболевания, его устойчивость к терапии и длительное течение заставляют многих врачей обращать внимание на причины, приводящие к развитию кандидной инфекции. Повышенный научный и практический интерес к данной проблеме обусловлен также тем, что в ряде случаев вульвовагинальный кандидоз является одной из причин развития тяжелой инфекционной патологии женских половых органов, плода и новорожденного.
В последние годы все чаще встречаются длительно текущие, рецидивирующие формы вульвовагинального кандидоза. В основном страдают женщины репродуктивного возраста, но заболевание может возникать в периоды мено-, постменопаузы и в детском возрасте.
Первый эпизод заболевания вагинальным кандидозом часто отмечается во время беременности. Вероятность колонизации грибами Candida и развития кандидоза возрастает именно в этот период. Лабораторно и клинически кандидоз обнаруживается не менее чем у 30% и 20% беременных соответственно. Особенно высок риск развития инфекционного процесса в последнем триместре беременности.
Антибиотики, наряду с гормональными контрацептивами, — одни из основных факторов риска. Развитию кандидоза способствует применение системных антибиотиков и препаратов местного действия, содержащих йод, клиндамицин и метронидазол. Антибактериальные средства выступают как предрасполагающий фактор только на фоне кандидоносительства, их влияние кратковременно и может привести к возникновению заболевания только в период применения препаратов.
В числе факторов риска выделяют различные средства контрацепции, прежде всего пероральные гормональные контрацептивы, а из них — препараты первого поколения с высоким содержанием эстрогенов. Внутриматочные средства в большей степени ассоциируются с бактериальными инфекциями, чем с кандидозом. Спермициды, в частности ноноксинол, используемые в сочетании с диафрагмой, также считаются фактором риска. Заболеваемость вагинальным кандидозом высока среди больных сахарным диабетом.
К факторам, предрасполагающим к рецидивированию кандидозного вульвовагинита, относят также чрезмерное употребление пищи, богатой углеводами; ношение облегающего нижнего белья, особенно из синтетических тканей, что приводит к повышению температуры и влажности на поверхности тела, то есть созданию благоприятных условий для развития грибковой флоры. Спринцевание, использование спреев, пены для ванн и гигиенических прокладок может вызывать аллергические реакции, способствующие колонизации грибов ряда Candida.
Определенное значение имеет половой путь передачи инфекции. Наиболее высокая заболеваемость вагинальным кандидозом отмечается среди женщин репродуктивного возраста. В своих исследованиях M. L. O’Connor, J. D. Sobel (1986) и I. W. Fong (1992) доказали, что у половых партнеров пациенток с рецидивирующей формой кандидоза грибы Candida определяли в 30-40% случаев в полости рта, в 26-30% — на слизистой оболочке полового члена, в 15% — в эякуляте. Передача инфекции в случае с рецидивирующей формой кандидоза половым путем доказана в 50% случаев.
На сегодняшний день накоплен немалый опыт в лечении вульвовагинального кандидоза, однако появившиеся сведения об этиологии, эпидемиологии и патогенезе заболевания внесли изменения в подходы к терапии. По результатам сравнительных исследований, лечение пероральными антимикотиками местного действия для исключения возможного источника реинфекции в кишечнике не способствует сокращению рецидивов. Использование эубиотиков для коррекции кишечного дисбиоза при вагинальном кандидозе не имеет научного обоснования, но, тем не менее, широко распространено во врачебной практике. Целесообразность лечения полового партнера допускается, но убедительно не доказана.
Неясность и вариабельность иммунологических изменений при хроническом вульвовагинальном кандидозе заставляет воздерживаться от общих рекомендаций по иммунокоррекции и отдавать предпочтение оценке иммунологического статуса в каждом случае заболевания. Зарубежные специалисты стремятся избегать иммунотропной терапии, объясняя такой подход феноменом «антигенной перегрузки» и нормализацией иммунологических сдвигов после курса противогрибковой терапии.
Приступая к лечению вульвовагинального кандидоза, следует помнить о том, что целью медикаментозного воздействия является, прежде всего, эрадикация возбудителя. Наличие характерных симптомов заболевания, наряду с лабораторным подтверждением, должны убеждать врача в том, что в первую очередь необходимо лечить не расстройство вагинального микроценоза и не предрасполагающие состояния, а инфекцию, вызванную Candida. Зачастую комплексные подходы, учитывающие массу сопутствующих факторов и предполагающие одновременное воздействие на них, приводят к необоснованной полипрагмазии, излишнему усложнению схемы лечения как для врача, так и для пациента, а иногда способствуют торпидному течению заболевания.
В настоящее время в соответствии с классификацией Л. С. Страчунского для лечения вульвовагинального кандидоза используют следующие противогрибковые препараты:
- препараты полиенового ряда — нистатин, леворин, амфотерицин В;
- препараты имидазолового ряда — кетоконазол, клотримазол, миконазол, бифоназол;
- прапараты триазолового ряда — флуконазол, интраконазол;
- гризеофульвин, флуцитзин, нитрофунгин, декамин, препараты йода и другие.
Одним из первых полиеновых антибиотиков в лечении кандидоза стали применять нистатин, он малотоксичен и, как правило, хорошо переносится больными, но почти не всасывается в желудочно-кишечном тракте, и большая часть его выделяется с калом. Биодоступность нистатина не превышает 3-5%. Нистатин применяют по 500 000 ЕД 4-5 раз в сутки в течение 10-14 дней.
Нередко для повышения эффективности лечения нистатин перорально сочетают с местным его введением в виде свечей по 100 000 ЕД в течение 7-14 дней. Нередко при использовании нистатина формируются нистатиноустойчивые штаммы Candida, но побочных реакций, как правило, не наблюдается.
До недавнего времени одним из эффективных препаратов считали леворин, однако он токсичен, обладает тератогенными свойствами, противопоказан при заболеваниях печени, желудочно-кишечного тракта и беременности. Препарат назначают по 500 000 ЕД 3-4 раза в сутки после еды в течение 10-15 дней. Эффективность применения леворина, как и нистатина, довольно низка. Эффективным, но высокотоксичным препаратом является амфотерицин В. Новый препарат этой группы — натамицин, к которому чувствительны большинство патогенных дрожжеподобных грибов, особенно Candida albicans. Натамицин малотоксичен, не вызывает раздражения кожи и слизистых оболочек и, что очень важно, может применяться при беременности и в период лактации. Назначают натамицин по следующей схеме: кишечно-растворимые таблетки — по 1 таблетке 4 раза в день в течение 5-10 дней; влагалищные свечи — по 1 свече на ночь в течение 6 дней; крем наносят на поверхность слизистых оболочек и кожи тонким слоем 2-3 раза в день. При применении данного препарата довольно высока частота рецидивов заболевания.
Для лечения генитального кандидоза применяют Пимафукорт — комбинированный препарат, в состав которого входят натамицин, неомицина сульфат и гидрокортизон. Препарат выпускается в виде крема и лосьона.
Высокоэффективный препарат из группы имидазолов — кетоконазол. Его механизм действия состоит в подавлении эргостерольного биосинтеза в клетке гриба. Прием препарата в высоких дозах дает кумулятивный эффект. Кроме того, могут наблюдаться такие побочные реакции, как тошнота, рвота. При длительном приеме отмечали случаи возникновения гепатита, алопеции, артралгии, гипертензии, тромбофлебита. Препарат оказывает угнетающее действие на функцию надпочечников, иммунную систему. Поэтому рекомендуемая доза препарата не должна превышать 400 мг в сутки в течение 5 дней. Противопоказаниями к назначению являются выраженные нарушения функции печени и почек, беременность, лактация.
Клотримазол тормозит синтез нуклеиновых кислот, липидов, полисахаридов клетки гриба, что, в свою очередь, приводит к повреждению клеточной оболочки и увеличению проницаемости лизосомальных мембран. Препарат выпускают в виде вагинальных таблеток, крема.
Некоторые авторы свидетельствуют о довольно высокой эффективности клотримазола при интравагинальном применении в течение 6 дней. Другие исследователи отмечают положительный эффект при однократном применении 500 мг Канестена в виде интравагинальных таблеток. Широкое применение получил вагинальный крем, содержащий 1% и 2% клотримазола. Препарат противопоказан в первом триместре беременности.
В последние годы широкое применение в лечении вульвовагинального кандидоза нашел флуконазол, который относится к новому классу триазольных соединений. Препарат угнетает биосинтез стеролов мембраны грибов, связывает группу гемазависимого от цитохрома Р450 фермента ланостерол-14-деметилазы грибковой клетки, нарушает синтез эргостерола, в результате чего избирательно ингибируется рост грибов. Побочные эффекты, как правило, отсутствуют.
Биодоступность флуконазола высока и достигает 94%. Он хорошо абсорбируется в желудочно-кишечном тракте, проникает через гистогематические барьеры. Важно отметить, что абсорбция препарата из кишечника не зависит от приема пищи. Учитывая длительный период полувыведения флуконазола из плазмы (около 30 часов), препарат можно назначать однократно. В настоящее время флуконазол является препаратом выбора для лечения острого и/или хронического вульвовагинального кандидоза и профилактики развития кандидоза у пациенток высокого риска.
Наиболее оптимальная доза флуконазола для лечения вагинального кандидоза — 150 мг однократно перорально, это определяет его преимущество перед другими антимикотическими средствами. Что касается профилактики возникновения вагинального кандидоза и его рецидивов, то универсальных рекомендаций не существует, все лечебные мероприятия сводятся к устранению или минимизации возможных факторов риска и своевременной эрадикации возбудителя.
Литература
- Прилепская В. Н., Анкирская А. С., Байрамова Г. Р., Муравьева В. В. Вагинальный кандидоз. М., 1997, 260 с.
- Сергеев А. Ю. Иммунитет при кандидозе // Иммунопатология, аллергология, инфектология, 1999, № 1, с. 81-86.
- Сергеев А. Ю., Сергеев Ю. В. Иммунопатогенез грибковых инфекций и иммунокоррекция. В кн.: Успехи отечественной иммунологии (под ред. А. В. Караулова). М., 2000.
- Atia W.A., Thin R. N. Cervical cytology in genital infection. // Br. J. Vener Dis. — 1975. — № 51 (5). — P. 331-2.
- Barbone F., Austin H., Louv W.C., Alexander W.J., A follow-up study of methods of contraception, sexual activity, and rates of trichomoniasis, candidiasis, and bacterial vaginosis.// Am. J. Obstet Gynecol — 1990 — 163 — P. 104-514.
- 6. Boeke A.J., Dekker J.H., Peerbooms P.G. A comparison of yield from cervix versus vagina for culturing Candida albicans and Trichomonas vaginalis. // Genitourin Med. 1993. -№ 69 (1). — P. 41-43.
- 7. Emmerson J., Gunputrao A., Hawkswell J., Dexter A., Sykes R., Searle S., Cross A., Nathan P.M. Sampling for vaginal candidosis: how good is it? // Int J STD AIDS. 1994. — № 5 (5). — P. 356-358.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Новый противогрибковый препарат Залаин для лечения острого вульвовагинального кандидоза
Новый противогрибковый препарат Залаин для лечения острого вульвовагинального кандидоза
 Современный взгляд на проблему и лечение кандидозных вульвовагинитов
Современный взгляд на проблему и лечение кандидозных вульвовагинитов
 Бактериальный вагиноз: некоторые аспекты этиологии, патогенеза, клиники, диагностики и лечения
Бактериальный вагиноз: некоторые аспекты этиологии, патогенеза, клиники, диагностики и лечения
 Молочница: кто виноват, и что делать?
Молочница: кто виноват, и что делать?