Эголанза 5 мг инструкция, аналоги и состав
| Показания: | Лікування шизофренії.Підтримання досягнутого клінічного ефекту під час тривалої терапії у пацієнтів, у яких спостерігалася відповідь на початкову терапію.Лікування маніакальних епізодів помірного та тяжкого ступеня.Профілактика повторних нападів у пацієнтів з біполярними розладами, у яких було отримано позитивну відповідь при лікуванні оланзапіном манії. |
| Форма випуска: | Таблетки, вкриті плівковою оболонкою, по 5 мг № 28 (7х4), № 56 (7х8) у блістерах |
| Производитель, страна: | ЗАТ Фармацевтичний завод ЕГІС, Угорщина |
| Действующее вещества: | 1 таблетка, вкрита плівковою оболонкою, містить 5 мг оланзапіну (що еквівалентно 7,03 мг оланзапіну дигідрохлориду тригідрату) |
| МНН: | Olanzapine |
| Регистрация: | UA/11344/01/01з 17.02.2016 по 17.02.2021. Приказ 104 від 17.02.2016 |
| Код АТХ: |
|
Склад:
діюча речовина: 1 таблетка, вкрита плівковою оболонкою, містить 5 мг або 7,5 мг, або 10 мг, або 15 мг, або 20 мг оланзапіну (що еквівалентно 7,03 мг або 10,55 мг, або 14,06 мг, або 21,09 мг, або 28,12 мг оланзапіну дигідрохлориду тригідрату відповідно);
допоміжні речовини: целюлоза мікрокристалічна, лактози моногідрат, гіпролоза (гідроксипропілцелюлоза), кросповідон, магнію стеарат;
склад оболонки: оpadry Y-1-7000 білий (гіпромелоза, титану діоксид (Е 171), макрогол 400), гіпромелоза, хіноліновий жовтий (Е 104).
Лікарська форма. Таблетки, вкриті плівковою оболонкою.
Основні фізико-хімічні властивості:
5 мг: жовтого кольору, продовгуваті, двоопуклі таблетки, вкриті плівковою оболонкою, без або майже без запаху, з рискою з одного боку, з гравіруванням стилізованої літери «Е» та цифрою «402» з іншого боку;
7,5 мг: жовтого кольору, круглі, двоопуклі таблетки, вкриті плівковою оболонкою, без або майже без запаху, з гравіруванням стилізованої літери «Е» та цифрою «403» з одного боку;
10 мг: жовтого кольору, круглі, двоопуклі таблетки, вкриті плівковою оболонкою, без або майже без запаху, з гравіруванням стилізованої літери «Е» та цифрою «404» з одного боку;
15 мг: жовтого кольору, круглі, двоопуклі таблетки, вкриті плівковою оболонкою, без або майже без запаху , з гравіруванням стилізованої літери «Е» та цифрою «405» з одного боку;
20 мг: жовтого кольору, круглі, двоопуклі таблетки, вкриті плівковою оболонкою, з гравіруванням стилізованої літери «Е» та цифрою «406» з одного боку.
Фармакотерапевтична група. Антипсихотичні засоби.
Код АТХ N05A H03.
Фармакологічні властивості.
Фармакодинаміка.
Оланзапін є антипсихотичним лікарським засобом з широким спектром фармакологічної дії, зумовленим впливом на різні рецептори. Виявлена спорідненість оланазпіну з деякими рецепторами (Ki; <100 nM) – серотоніну 5НТ2А/2С, 5-НТ3, 5-НТ6; допаміну D1, D2, D3, D4, D5; холінергічними мускариновими рецепторами m1-m5; α-1-адренергічним рецептором та гістаміновим рецептором Н1. Оланзапін селективно зменшує збудливість мезолімбічних (А10) допамінергічних нейронів, проявляючи при цьому незначний вплив на стріарні (А9) шляхи, пов'язані з моторною функцією. Оланзапін послаблює зобумовлену реакцію уникнення, що свідчить про його нейролептичні властивості, у дозах, нижчих за ті, що спричиняють каталепсію, – побічний ефект, пов’язаний з порушенням рухомості. На відміну від інших антипсихотичних засобів, оланзапін посилює відповідь при проведенні «анксіолітичного» тесту.
Фармакокінетика.
Оланзапін добре всмоктується після перорального прийому, максимальна концентрація його у плазмі крові досягається через 5-8 годин. Прийом їжі не впливає на всмоктування оланзапіну. Абсолютна біодоступність після перорального застосування відносно внутрішньовенного застосування не була встановлена.
Оланзапін метаболізується у печінці шляхом кон'югації та окиснення. Основним циркулюючим метаболітом є 10-N-глюкуронід, який не проникає крізь гематоенцефалічний бар'єр. Цитохроми P450-CYP1A2 і P450-CYP2D6 сприяють утворенню метаболітів N-дезметилу і 2-гідроксиметилу; у дослідженнях на тваринах обидва метаболіти проявляли значно меншу фармакологічну активність in vivo, ніж оланзапін. Переважаюча фармакологічна активність зумовлена первинним оланзапіном. Після перорального застосування середній період напіввиведення оланзапіну у здорових пацієнтів варіює залежно від статі та віку хворого.
У здорових осіб літнього віку (від 65 років); порівняно з молодшими особами, середній період напіввиведення був подовжений (51,8 порівняно з 33,8 години), а кліренс препарату зменшений (17,5 порівняно з 18,2 л за годину). Варіабельність фармакокінетичних параметрів, що спостерігалася у пацієнтів літнього віку, знаходилася у межах діапазону, визначеного для молодших осіб. У 44 хворих на шизофренію віком від 65 років дози від 5 до 20 мг/добу не впливали на характер побічних реакцій.
У жінок порівняно з чоловіками середній період напіввиведення був дещо подовжений (36,7 порівняно з 32,3 години), а кліренс препарату зменшений (18,9 порівняно з 27,3 л за годину). Однак оланзапін (5-20 мг) продемонстрував аналогічний профіль безпеки як у жінок (n = 467), так і в чоловіків (n = 869).
У пацієнтів з порушенням функції нирок (кліренс креатиніну < 10 мл/хв) порівняно зі здоровими особами була відсутня істотна різниця у середньому періоді напіввиведення (37,7 порівняно з 32,4 години) та кліренсі препарату (21,2 порівняно з 25,0 л за годину). Аналіз масового балансу показав, що приблизно 57 % оланзапіну з радіоактивною міткою були присутні у сечі головним чином у вигляді метаболітів.
У пацієнтів зі слабким порушенням функції печінки, які палять, середній період напіввиведення (39,3 години) був подовжений, а плазмовий кліренс (18,0 л за годину) зменшений порівняно зі здоровими особами, які не палять (48,8 години і 14,1 л за годину, відповідно).
В осіб, які не палять, порівняно з особами, які мають звичку палити (чоловіки і жінки), середній період напіввиведення подовжувався (38,6 порівняно з 30,4 години), а кліренс препарату зменшувався (18,6 порівняно з 27,7 л за годину).
Плазмовий кліренс оланзапіну зменшується в осіб літнього віку порівняно з молодими, у жінок порівняно з чоловіками і в осіб, які не палять, порівняно з тими, що мають звичку палити. Проте ступінь впливу віку, статі або паління на кліренс і період напіввиведення оланзапіну незначний порівняно з загальною варіабельністю між особами.
Фармакокінетичні властивості препарату не залежать від раси.
Рівень зв'язування оланзапіну з протеїнами плазми крові становить приблизно 93 % для концентрації у межах від 7 нг/мл до 1 000 нг/мл. Оланзапін зв'язується переважно з альбуміном і a1-кислим глікопротеїном.
Клінічні характеристики.
Показання.
Лікування шизофренії.
Підтримання досягнутого клінічного ефекту під час тривалої терапії у пацієнтів, у яких спостерігалася відповідь на початкову терапію.
Лікування маніакальних епізодів помірного та тяжкого ступеня.
Профілактика повторних нападів у пацієнтів з біполярними розладами, у яких було отримано позитивну відповідь при лікуванні оланзапіном манії.
Протипоказання.
Підвищена чутливість до діючої речовини або до будь-якої з допоміжних речовин препарату; відомий ризик закритокутової глаукоми.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
На метаболізм оланзапіну можуть впливати інгібітори чи індуктори ізоформ цитохрому Р450, особливо на активність CYP1A2. Паління або застосування карбамазепіну підвищували метаболізм оланзапіну, що може призвести до зниження концентрації оланзапіну. Відомі інгібітори активності CYP1A2 можуть знижувати кліренс оланзапіну. Інгібування метаболізму оланзапіну не відзначалося при застосуванні препарату з трициклічними антидепресантами (CYP2D6), варфарином (CYP2C19), теофіліном (CYP1A2) або діазепамом (CYP3A4, CYP2C19). Не було відзначено взаємодії оланзапіну при призначенні з літієм або біпериденом. Терапевтичний моніторинг рівнів вальпроату у плазмі крові не виявив необхідності корекції дози вальпроату при супутньому призначенні з оланзапіном. При застосуванні етанолу разом з оланзапіном можливі додаткові фармакологічні впливи, такі як підвищена седація. Флуоксетин, разова доза антацидів, що містять алюміній та магній, або циметидину не впливали на пероральну біодоступність оланзапіну. Оланзапін може виявляти антагонізм до ефектів прямих та непрямих агоністів допаміну. Додаткове призначення активованого вугілля знижувало пероральну біодоступність оланзапіну на 50-60 %, тому його не слід застосовувати протягом 2 годин до прийому і 2 годин після прийому оланзапіну. Флуоксамін, інгібітор CYP1A2, знижує метаболізм оланзапіну. Це призводить до середнього зростання Cmax після прийому флуоксаміну на 54 % серед жінок, які не палять, та на 77 % серед чоловіків, які палять. Середнє зростання AUC оланзапіну становить 52 % та 108 % відповідно. Для пацієнтів, які застосовують флуоксамін або будь-які інші інгібітори CYP1A2, наприклад ципрофлоксацин, необхідно призначати знижені дози оланзапіну. Необхідно розглянути можливість зниження дози оланзапіну, якщо ініційовано лікування інгібітором CYP1A2.
Інгібітори CYP2D6. Флуоксетин (60 мг на 1 прийом або 60 мг щоденно протягом 8 днів) спричиняє середнє зростання максимальної концентрації оланзапіну на 16 % та середнє зниження кліренсу оланзапіну на 16 %. Значення впливу цих факторів мале порівняно з загальною індивідуальною змінюваністю, тому зміни дозування зазвичай не рекомендовані.
Супутнє застосування оланзапіну з антипаркінсонічними препаратами пацієнтам із хворобою Паркінсона та деменцією не рекомендується.
Слід з обережністю призначати оланзапін з іншими препаратами з відомим ризиком підвищення інтервалу QTc.
Потенційна здатність оланзапіну взаємодіяти з іншими лікарськими засобами.
Антигіпертензивні засоби. Оланзапін через потенційну здатність спричиняти гіпотензії може посилювати ефекти певних антигіпертензивних засобів.
Леводопа та агоністи допаміну. Оланзапін може проявляти антагонізм до ефектів леводопи та агоністів допаміну.
Іміпрамін. Разові дози оланзапіну не впливають на фармакокінетику іміпраміну або його активного метаболіту дезипраміну.
Особливості застосування.
Під час лікування антипсихотичними засобами поліпшення пригніченого стану пацієнту може зайняти від кількох днів до кількох тижнів. Протягом цього періоду необхідний ретельний моніторинг пацієнтів.
Психоз, пов’язаний з деменцією та/або розладами поведінки. Оланзапін не призначений для лікування психозів, пов’язаних з деменцією та/або порушенням поведінки, а також не рекомендується для застосування даним пацієнтам у зв’язку з підвищенням летальності та ризику цереброваскулярних випадків. У ході плацебо-контрольованих клінічних досліджень (тривалістю 6-12 тижнів) за участю літніх пацієнтів (середній вік 78 років), які страждають на психози, пов’язані з деменцією та/або порушенням поведінки, кількість летальних випадків була у 2 рази вища у пацієнтів, які приймали оланзапін, порівняно із плацебо (3,5 % проти 1,5 % відповідно). Висока летальність не була пов’язана з величиною застосовуваних доз оланзапіну (середня добова доза становить 4,4 мг) або з тривалістю лікування. Фактори ризику, які можуть спричинити підвищення летальності, включають вік від 65 років, дизфагію, заспокоєння, недоїдання та зневоднення, легеневі стани (пневмонія з або без аспірації), супутнє застосування бензодіазепінів. Проте випадки летальності були вищі при терапії оланзапіном, ніж при прийомі плацебо, незалежно від факторів ризику.
У ході клінічних досліджень спостерігалися випадки цереброваскулярних побічних реакцій (інсульт, транзиторний ішемічний інсульт), у тому числі з летальним наслідком. Кількість цереброваскулярних побічних реакцій була у 3 рази вища у пацієнтів, які приймали оланзапін, порівняно із плацебо (1,3 % проти 0,4 % відповідно). Усі пацієнти, які приймали оланзапін або плацебо і у яких спостерігалися цереброваскулярні побічні реакції, мали фактори ризику. Вік від 75 років та судинний/змішаний тип деменції були ідентифіковані як фактори ризику цереброваскулярних побічних реакцій при терапії оланзапіном. Ефективність оланзапіну не була встановлена у ході даних досліджень.
Хвороба Паркінсона. Не рекомендоване застосування оланзапіну у терапії психозів, що асоційовані з агоністами допаміну. Не рекомендоване супутнє застосування оланзапіну та протипаркінсонічних лікарських засобів пацієнтам із хворобою Паркінсона та деменцією. У ході клінічних досліджень дуже часто спостерігалось погіршення симптоматики хвороби Паркінсона та галюцинацій, частіше, ніж при прийомі плацебо; при лікуванні психотичних симптомів терапія оланзапіном не була більш ефективною, порівняно із застосуванням плацебо. З самого початку цих досліджень, від пацієнтів вимагалось постійне застосовування найменшої ефективної дози антипаркінсонічних лікарських засобів (агоністів допаміну), а також застосовування тих самих антипаркінсонічних лікарських засобів і доз протягом усього дослідження. Терапію оланзапіном було розпочато з дози 2,5 мг/добу, яку збільшували шляхом титрування до максимального показника 15 мг/добу.
Нейролептичний злоякісний синдром (НЗС). НЗС – це потенційно летальний симптомокомплекс, описаний у зв’язку з антипсихотичними препаратами. Рідко повідомлялося про випадки НЗС, пов’язані із застосуванням оланзапіну. Клінічними проявами НЗС є гіперпірексія, м’язова ригідність, втрата свідомості та симптоми серцевої нестабільності (нерегулярний пульс або артеріальний тиск, тахікардія, підвищене потовиділення та серцева аритмія). Додаткові ознаки можуть включати підвищений рівень креатинінфосфокінази, міоглобінурію (рабдоміоліз) та гостру ниркову недостатність. Клінічний прояв НЗС або наявність гіпертермії без клінічного прояву НЗС потребує негайної відміни всіх антипсихотичних засобів, включаючи оланзапін.
Гіперглікемія і цукровий діабет. Нечасто повідомлялося про гіперглікемію та/або розвиток цукрового діабету або погіршення перебігу вже існуючого, асоційованого з кетоацидозом або діабетичною комою, а також про летальні випадки. У деяких випадках повідомлялося про попереднє підвищення маси тіла, що могло бути фактором ризику.
Рекомендовано проводити відповідний клінічний моніторинг пацієнтів з цукровим діабетом та пацієнтів з факторами ризику розвитку цукрового діабету, зокрема вимірювати рівень глюкози у крові на початку лікування, через 12 тижнів, а також щорічно у подальшому. Пацієнти, які отримують лікування антипсихотичними засобами, включаючи оланзапін, повинні бути під наглядом для виявлення симптомів гіперглікемії (таких як полідипсія, поліурія, поліфагія та слабкість). У пацієнтів з цукровим діабетом та пацієнтів з факторами ризику розвитку цукрового діабету необхідно регулярно перевіряти рівень контролю глюкози. Необхідно контролювати масу тіла, наприклад на початку лікування, через 4 тижні, через 8 тижнів та через 12 тижнів, а також 1 раз на квартал у подальшому.
Антихолінергічна активність. У ході клінічних досліджень виявлено низьку частоту антихолінергічних явищ. Однак через обмеженість клінічного досвіду застосування оланзапіну пацієнтам із супутніми захворюваннями слід бути обережними при призначенні препарату пацієнтам із гіпертрофією простати, паралітичною кишковою непрохідністю або подібними станами.
Показники печінкової функції. При застосуванні оланзапіну часто спостерігалися транзиторні асимптоматичні підйоми рівня печінкових трансаміназ АлАТ та АсАТ, особливо на початку лікування. Пацієнтам із підвищеним рівнем АлАТ та/чи АлАТ, ознаками та симптомами порушення діяльності печінки, станами, пов’язаними з печінковою недостатністю, а також пацієнтам, які приймають потенційно гепатотоксичні препарати, Еголанзу призначають з обережністю. При виявленні гепатиту (включаючи гепатоцелюлярне, холестатичне чи змішане ураження печінки) оланзапін необхідно відмінити.
Нейтропенія. Оланзапін необхідно призначати з обережністю при низькому рівні лейкоцитів та/або нейтрофілів з будь-якої причини, пацієнтам, які отримують лікування препаратами, що можуть спричинити нейтропенію, пацієнтам, які мають в анамнезі медикаментозне пригнічення/токсичне ураження кісткового мозку, пацієнтам із пригніченням кісткового мозку, спричиненим супутніми захворюваннями, опроміненням чи хіміотерапією, та пацієнтам із гіпереозинофілією та мієлопроліферативним захворюванням. Нейтропенія є частим побічним ефектом при сумісному застосуванні вальпроату та оланзапіну.
Припинення терапії. При різкому припиненні терапії дуже рідко (≥ 0,01 % та 0,1 %) повідомлялося про гострі симптоми, зокрема про надмірне потовиділення, безсоння, тремор, роздратованість, нудоту або блювання.
QT-інтервал. У ході клінічних досліджень оланзапін не спричинював довготривалої пролонгації абсолютних інтервалів QT та QTс. Однак, як і при лікуванні іншими антипсихотичними засобами, призначати оланзапін у комбінації з препаратами, які можуть спричинити пролонгацію інтервалу QTс, слід з обережністю, особливо пацієнтам літнього віку, пацієнтам із вродженим синдромом пролонгації інтервалу QT, застійною серцевою недостатністю, гіпертрофією серця, гіпокаліємією чи гіпомагнезіємією.
Тромбоемболія. Нечасто повідомлялося про тимчасовий зв’язок між лікуванням оланзапіном та випадками розвитку венозної тромбоемболії (≥ 0,1 % – < 1 %). Причинно-наслідковий зв’язок між лікуванням оланзапіном та розвитком венозної тромбоемболії не встановлено. Однак, беручи до уваги те, що у пацієнтів із шизофренією часто розвивається схильність до тромбоемболії, необхідно враховувати усі можливі фактори ризику, наприклад іммобілізацію пацієнта, та вживати всіх необхідних попереджувальних заходів.
Загальна дія на ЦНС. Враховуючи переважний вплив оланзапіну на ЦНС, необхідно проводити додаткові застережні заходи при прийомі оланзапіну в поєднанні з іншими препаратами центральної дії, включаючи вживання алкоголю.
Епілептичні напади. Оланзапін необхідно з обережністю застосовувати пацієнтам з епілептичними нападами в анамнезі або пацієнтам, у яких наявні фактори, що знижують пороги нападів. Рідко повідомлялося про випадки епілептичних нападів при лікуванні оланзапіном. У більшості цих випадків пацієнти мали в анамнезі епілептичні напади або ризик їх виникнення був підвищений.
Пізня дискінезія. При прийомі оланзапіну спостерігалася статистично значущо більш низька частота виникнення дискінезії, спричиненої лікуванням. Через зростаючий ризик розвитку пізньої дискінезії при тривалому прийомі антипсихотичних препаратів необхідне узгоджене зниження дози або повна відміна препарату при появі у пацієнта симптомів пізньої дискінезії. З часом ці симптоми можуть посилюватися або навіть з’являтися після припинення лікування.
Ортостатична гіпотензія. Нечастоповідомлялося про випадки ортостатичної гіпотензії у пацієнтів літнього віку. Як і при лікуванні іншими антипсихотичними лікувальними зазобами, під час застосування оланзапіну рекомендується періодичне вимірювання артеріального тиску пацієнтам віком від 65 років.
Раптова зупинка серця. Повідомлялося про випадки раптової зупинки серця. Ризик раптової зупинки серця у пацієнтів, які отримували лікування оланзапіном, підвищувався майже вдвічі порівняно з пацієнтами, які не застосовували антипсихотичні препарати. Ризик при застосуванні оланзапіну відповідає такому при застосуванні атипових антипсихотичних засобів, що були включені до об’єднаного аналізу.
Лактоза. Таблетки Еголанза містять лактозу, тому їх не можна призначати хворим, які мають спадкову непереносимість лактози, дефіцит лактази (The Lapp lactose deficiency) або синдром глюкозо-галактазної мальабсорбції.
Допамінергічний антагонізм. Оланзапін invitro виявляє антагонізм до допаміну та теоретично може протидіяти ефектам леводопи та агоністам допаміну, як і інші антипсихотичні засоби.
Глюкоза. Оланзапін спричиняє більші зміни рівня глюкози порівняно з плацебо. Різниця у змінах значень між оланзапіном та плацебо була більшою у пацієнтів із симптомами дизрегуляції глюкози в анамнезі (включаючи пацієнтів з цукровим діабетом або пацієнтів із проявами гіперглікемії). У цих пацієнтів спостерігалося значне підвищення HbA1с порівняно з групою плацебо.
Відсоткове співвідношення пацієнтів, у яких змінився рівень глюкози з нормального або граничного до високого, постійно збільшувалося.
В аналізах пацієнтів, які пройшли 9–12-місячну терапію оланзапіном, підвищений рівень глюкози у крові знижувався через 6 місяців.
Зміни рівня ліпідів. Небажані зміни рівнів ліпідів можуть спостерігатися у пацієнтів, які лікуються оланзапіном. Зміни рівня ліпідів слід лікувати належним чином у пацієнтів із дисліпідемією та у пацієнтів із факторами ризику розвитку порушень обміну ліпідів. У пацієнтів, які отримують лікування антипсихотичними засобами, включаючи оланзапін, необхідно регулярно перевіряти рівні ліпідів у крові, наприклад на початку лікування, через 12 тижнів, а також кожні 5 років у подальшому.
У пацієнтів, які приймали оланзапін, спостерігалося підвищення рівня загального холестерину, ліпопротеїдів низької щільності і тригліцеридів порівняно з групою плацебо.
Значне підвищення рівня ліпідів (загального холестерину, ліпопротеїдів низької щільності, тригліцеридів) спостерігалося частіше у пацієнтів без порушення обміну ліпідів в анамнезі.
Не спостерігалося статистично підтверджених відмінностей підвищення ліпопротеїдів високої щільності між пацієнтами, які приймали оланзапін, та пацієнтами, які приймали плацебо.
Кількісне співвідношення пацієнтів, у яких змінився рівень загального холестерину, ліпопротеїдів низької щільності або тригліцеридів з нормального або граничного рівня до високого або змінився рівень ліпопротеїдів високої щільності з нормального або граничного до низького, було більшим у ході довготривалих досліджень (не менше 48 тижнів) порівняно з таким при короткотермінових дослідженнях. У пацієнтів, які пройшли 12-місячну терапію, рівень загального холестерину не зростав після 4-6 місяців.
Суїцид. Можливість спроб суїциду притаманна як для пацієнтів із шизофренією, так і для пацієнтів із біполярним розладом I типу, у зв’язку з чим потрібно ретельно спостерігати за пацієнтами, які знаходяться в зоні високого ризику та отримують терапію оланзапіном. З метою зниження імовірності передозування у пацієнтів потрібно виписувати оланзапін у таблетках малими кількостями, які необхідні для забезпечення належного лікувального ефекту.
Маса тіла.Перед початком терапії оланзапіном слід враховувати потенційні наслідки підвищення маси тіла пацієнта. Пацієнти, які отримують лікування оланзапіном, повинні контролювати масу тіла.
Монотерапія оланзапіном дорослих. У пацієнтів, які отримували терапію оланзапіном, спостерігалося у середньому підвищення маси тіла на 2,6 кг порівняно із втратою маси тіла в середньому на 0,3 кг у групі плацебо при медіані застосування 6 тижнів; у 22,2 % пацієнтів із тих, які отримували терапію оланзапіном, спостерігалося підвищення маси тіла не менше ніж на 7 % маси на початку лікування порівняно з 3 % пацієнтів групи плацебо при медіані застосування 8 тижнів; у 4,2 % пацієнтів спостерігалося збільшення маси тіла принаймні на 15 % маси на початку лікування порівняно з 0,3 % пацієнтів групи плацебо при медіані застосування 12 тижнів. Клінічно значуще збільшення маси тіла спостерігалося у всіх категорій пацієнтів за ІМТ (індекс маси тіла). Припинення терапії через збільшення маси тіла відзначалося у 0,2 % пацієнтів, які отримували лікування оланзапіном, порівняно з 0 % пацієнтів з групи плацебо.
У ході довготривалих клінічних досліджень (не менше 48 тижнів) середнє збільшення маси тіла у пацієнтів було 5,6 кг (при медіані застосування 573 дні; N=2021). Кількість пацієнтів, у яких спостерігалося збільшення маси тіла не менш ніж на 7 %, 15 % або 25 % початкової маси, при довготривалому застосуванні оланзапіну становила 64 %, 32 % та 12 % відповідно. Припинення терапії через збільшення маси тіла відзначалося у 0,4 % пацієнтів, які отримували лікування оланзапіном протягом не менш ніж 48 тижнів.
Дисфагія. Порушення езофагальної моторики та задишка були асоційовані з прийомом антипсихотичних засобів. Аспіраційна пневмонія була частою причиною захворюваності та летальності у пацієнтів із хворобою Альцгеймера. Оланзапін не схвалений для лікування пацієнтів із хворобою Альцгеймера.
Регуляція температури тіла. Порушення здатності тіла знижувати свою температуру спостерігалося у зв’язку із антипсихотичними засобами. Рекомендовано зважати на цей факт при призначенні оланзапіну пацієнтам, які знаходяться в умовах, що можуть призвести до підвищення температури тіла, таких як посилені тренування, перебування в умовах екстремальних температур, супутнє застосування засобів з антихолінергічною активністю або стан дегідратації.
Застосування пацієнтам, які мають супутні захворювання. Клінічний досвід застосування оланзапіну пацієнтам із певними захворюваннями обмежений. Оланзапін посилює in vitro афінність до мускаринових рецепторів. У ході премаркетингових клінічних досліджень оланзапіну його застосування було асоційоване із запорами, відчуттям сухості в роті, тахікардією та іншими побічними явищами, що, можливо, пов’язані з холінергічним антагонізмом. Подібні побічні реакції нечасто вимагали припинення терапії оланзапіном, але необхідно з обережністю застосовувати оланзапін пацієнтам із клінічно значущою гіпертрофією простати, вузькокутовою глаукомою, паралітичною непрохідністю кишечнику в анамнезі або зі спорідненими станами, які спричинені холінергічним антагонізмом та можуть погіршуватися у присутності оланзапіну. У ході 5 плацебо-контрольованих досліджень оланзапіну у пацієнтів літнього віку із психозом, пов’язаним з деменцією (n=1184), повідомлялося про такі побічні реакції, пов’язані із терапією, із частотою виникнення не менше 2 % та зі значущо більш високою частотою виникнення порівняно з пацієнтами групи плацебо: падіння, сонливість, периферичні набряки, порушення ходи, нетримання сечі, летаргія, збільшення маси тіла, астенія, пірексія, пневмонія, відчуття сухості в роті та зорові галюцинації. Рівень припинення терапії через побічні явища був вищий у групі, яка отримувала оланзапін, порівняно з плацебо (13 % порівняно з 7 % відповідно). У пацієнтів літнього віку із психозом, пов’язаним з деменцією, які отримують оланзапін, вищий рівень летальних випадків. Оланзапін не показаний для лікування пацієнтів літнього віку із психозом, пов’язаним з деменцією. Оланзапін не застосовували у достатній кількості випадків пацієнтам із нещодавнім інфарктом міокарда або нестабільним серцевим захворюванням. Слід з обережністю застосовувати оланзапін для лікування пацієнтів із серцевими захворюваннями через ризик виникнення ортостатичної гіпотензії.
Лабораторні дослідження. Рекомендується контролювати глюкозу натще та ліпідний профіль на початку лікування та періодично під час лікування.
Гіперпролактинемія. Як і інші засоби з властивостями антагоністів допамінових рецепторів D2, оланзапін підвищує в крові рівні пролактину, і це підвищення зберігається при тривалому застосуванні. Гіперпролактинемія може пригнічувати гіпоталамічний гормон GnRH, результатом чого є зниження секреції пітуїтарного гонадотропіну. Це, в свою чергу, може інгібувати репродуктивну функцію шляхом порушення гонадного сперматогенезу як у чоловіків, так і у жінок. Повідомлялося про галакторею, аменорею, гінекомастію та імпотенцію у пацієнтів, які отримували препарати, що підвищували рівень пролактину. Довготривала гіперпролактинемія, асоційована із гіпогонадизмом, може призвести до зниження щільності кісток як у чоловіків, так і у жінок.
Додаткові дослідження/лабораторні дані. У ході деяких досліджень на тваринах спостерігалася нейтропенія, асоційована з прийомом інших психотропних компонентів, та лейкопенія, асоційована із прийомом оланзапіну. Не було ознак ризику виникнення клінічно значущої нейтропенії, пов’язаної із лікуванням оланзапіном, у премаркетинговій базі даних оланзапіну.
Постмаркетингові звіти. Звіти про побічні реакції з моменту виходу оланзапіну на ринок, які були тимчасово пов’язані (але не обов’язково спричинені) з терапією оланзапін, включали нейтропенію.
Токсикологічні дослідження на тваринах. Під час досліджень оланзапіну на тваринах основними гематологічними результатами були оборотна периферична цитопенія в окремих особин собак при дозуванні 10 мг/кг (у 17 разів більша доза за максимальну рекомендовану денну пероральну дозу для людини при розрахунку дози у мг/м2 поверхні тіла), дозозалежне зниження кількості лімфоцитів і нейтрофілів у мишей і лімфопенія у щурів. У кількох собак, які отримували дози 10 мг/кг, розвинулась оборотна нейтропенія та/або оборотна гемолітична анемія у період між 1 і 10 місяцями лікування. Дозозалежне зниження кількості лімфоцитів і нейтрофілів було відзначалося в мишей, що отримували дозу 10 мг/кг (дорівнює дворазовій максимальній рекомендованій щоденній пероральній дозі для людини при розрахунку дози у мг/м2 поверхні тіла) у ході досліджень тривалістю 3 місяці. Неспецифічна лімфопенія, відповідно до зниження приросту маси тіла, спостерігалася у щурів, які отримували дозу 22,5 мг/кг (у 11 разів більша за максимальну рекомендовану щоденну пероральну дозу для людини при розрахунку дози у мг/м2 поверхні тіла) протягом 3 місяців або 16 мг/кг (у 8 разів більша за максимальну рекомендовану щоденну пероральну дозу для людини при розрахунку дози у мг/м2 поверхні тіла) протягом 6 або 12 місяців. Ніяких доказів цитотоксичності для кісткового мозку не було для жодного з вивчених видів. Клітини кісткового мозку були нормоцелюлярні або гіперцелюлярні, що свідчитить про те, що зниження циркулюючих клітин крові було, ймовірно, пов’язано з периферичними (не пов’язаними з кістковим мозком) факторами.
Застосування у період вагітності або годування груддю.
Відсутні адекватні і добре контрольовані дослідження дії оланзапіну на вагітних. Оскільки існуючий досвід лікування людей оланзапіном обмежений, оланзапін у період вагітності необхідно застосовувати тільки тоді, коли очікувані результати виправдовують можливий ризик для плода.
У новонароджених, матері яких приймали антипсихотичні лікарські засоби (включаючи оланзапін) протягом ІІІ триместру вагітності, існує ризик виникнення побічних реакцій, включаючи екстрапірамідні порушення та/або синдром відміни, симптоми яких можуть після народження змінюватися за силою та тривалістю. Повідомлялося про ажитацію, артеріальна гіпертензія, артеріальна гіпотензія, тремор, сонливість, респіраторний дистрес-синдром або розлад харчування. Тому необхідно контролювати стан новонароджених.
При дослідженні здорових жінок, які годували груддю, оланзапін було виявлено у грудному молоці. Середня доза для немовляти (мг/кг) без ризику для нього оцінювалася як 1,8 % від материнської дози (мг/кг). Пацієнткам рекомендується не годувати немовлят груддю, якщо вони приймають оланзапін.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Досліджень впливу оланзапіну на швидкість реакції при керуванні автотранспортом або роботі з іншими механізмами не проводилося. Оскільки оланзапін може спричинити сонливість та запаморочення, пацієнтів слід попередити про небезпеку, пов’язану з експлуатацією машин, включаючи автотранспортні засоби.
Спосіб застосування та дози.
Дорослі.
Шизофренія. Рекомендована початкова доза оланзапіну становить 10 мг 1 раз на добу.
Маніакальні епізоди. Рекомендована початкова доза оланзапіну як монотерапії становить 15 мг на добу або 10 мг на добу у комбінації з літієм чи вальпроатом.
Профілактика повторних нападів у пацієнтів з біполярними розладами. Рекомендована початкова доза становить 10 мг на добу. Пацієнти з біполярними розладами, які отримували оланзапін для лікування маніакальних епізодів, продовжують отримувати оланзапін у тому ж дозуванні і для профілактики повторних нападів. У разі розвитку нового маніакального, депресивного або змішаного епізоду лікування необхідно продовжувати (у разі необхідності оптимізувавши дозу) разом із підтримуючою терапією для лікування симптомів порушення настрою, якщо є клінічна необхідність.
Лікування шизофренії, маніакальних епізодів та попередження рецидивів біполярного розладу. Щоденну дозу визначають на підставі клінічного статусу в діапазоні від 5 до 20 мг на добу. Збільшення рекомендованої початкової дози проводити з інтервалами не менше 24 годин лише після клінічного обстеження. Оланзапін застосовувати незалежно від прийому їжі, оскільки вживання їжі не впливає на абсорбцію препарату. При відміні препарату завершення терапії слід проводити поступово.
Пацієнти літнього віку. Призначення меншої початкової дози (5 мг на добу) зазвичай не потрібне. Необхідність призначення меншої початкової дози потрібно розглядати для пацієнтів віком від 65 років при наявності клінічних факторів.
Пацієнти, які мають ниркову та/або печінкову недостатність. Меншу початкову дозу (5 мг на добу) можна призначати таким пацієнтам. У разі наявності помірної печінкової недостатності (цироз, класи недостатності А або В за шкалою Чайлда-П’ю) початкова доза повинна становити 5 мг, і підвищувати дозу необхідно з обережністю.
Меншу початкову дозу можна призначати пацієнтам з комбінацією факторів (жіноча стать, літній вік, відсутність звички до паління), які можуть знижувати метаболізм оланзапіну. Підвищення дози таким пацієнтам, якщо це показано, потрібно здійснювати поступово, з обережністю.
Пацієнтам з комбінацією факторів слід спочатку призначати найнижчу дозу (5 мг) та здійснювати моніторинг їх стану протягом кількох наступних діб. Якщо покращення стану відсутнє, доза можна збільшити до 10 мг за умови моніторингу стану пацієнта протягом кількох днів після підвищення дози. Підвищення дози може продовжуватися, як описано вище, до досягнення максимальної дози 20 мг.
Діти.
Оланзапін не показаний для лікування дітей та підлітків (віком до 18 років). Дослідження пацієнтів віком 13-17 років показали різні побічні реакції, а саме: збільшення маси тіла, зміни метаболічних параметрів та збільшення рівня пролактину. Результати, що були пов’язані з цими побічними діями, не досліджувались і залишаються невідомими.
Передозування.
Симптоми. Дуже поширені – тахікардія, ажитація/агресивність, дизартрія, різні екстрапірамідні симптоми та знижений рівень свідомості, можлива кома.
Іншими значними ускладненнями передозування є делірій, судоми, кома, можливість нейролептичного злоякісного синдрому, пригнічення дихання, аспірація, артеріальна гіпертензія або гіпотензія, серцева аритмія (< 2 % випадків передозування) та кардіопульмональний шок. Летальні наслідки відзначалися при гострому передозуванні на рівні 450 мг, але були й випадки виживання після гострого передозування після прийому 2 г.
Лікування. Специфічний антидот оланзапіну відсутній. Не рекомендуються препарати, що спричиняють блювання. Рекомендовано стандартні процедури при передозуванні (наприклад промивання шлунка, прийом активованого вугілля). Було виявлено, що супутній прийом активованого вугілля зменшує біодоступність оланзапіну при пероральному прийомі на 50-60 %.
Відповідно до клінічних проявів слід налагодити симптоматичне лікування та моніторинг життєво важливих функцій, включаючи лікування артеріальної гіпотензії та циркуляторної недостатності, а також підтримання дихання. Не слід застосовувати епінефрин, допамін та інші симпатоміметики з дією, характерною для бета-агоністів, оскільки бета-стимуляція може посилити прояви артеріальної гіпотензії. Для виявлення можливих аритмій необхідний моніторинг серцевої судинної системи. Ретельний медичний нагляд та моніторинг має тривати до повного одуження пацієнта.
Побічні реакції.
Найбільш частими побічними реакціями (спостерігалися у ≥ 1% пацієнтів), пов’язаними із застосуванням оланзапіну в ході клінічних досліджень, були такі: сонливість, збільшення маси тіла, еозинофілія, підвищення рівнів пролактину, холестеролу (холестерину), глюкози та тригліцеридів у крові, глюкозурія, підвищення апетиту, запаморочення, акатизія, паркінсонізм, лейкопенія, нейтропенія, дискінезія, ортостатична гіпотензія, антихолінергічні ефекти, транзиторне асимптоматичне підвищення печінкових трансаміназ, висипання, астенія, стомлюваність, гіпертермія, артралгія, підвищення рівня алкалінфосфатази, гаммаглутамілтрансферази, сечової кислоти, креатинфосфокінази та набряки.
У таблиці підсумовано основні побічні реакції та їхня частота, визначені у ході клінічних досліджень та/або на основі постмаркетингового досвіду.
Дуже часто (≥ 1/10), часто (≥ 1/100 та < 1/10), нечасто (≥ 1/1000 та < 1/100), рідко (≥ 1/10000 та < 1/1000), дуже рідко (< 1/10000), частота невідома (частоту не можна встановити на основі наявних даних).
Таблиця
|
Дуже часто |
Часто |
Нечасто |
Рідко |
|||
|
Порушення з боку системи кровотворення та лімфатичної системи |
||||||
|
Еозинофілія, лейкопенія10, нейтропенія10 |
Тромбоцитопенія11 |
|||||
|
Порушення з боку імунної системи |
||||||
|
Гіперчутливість11 |
||||||
|
Порушення обміну речовин та розлади травлення |
||||||
|
Збільшення маси тіла1 |
Підвищення рівня холестерину2,3, підвищення рівня глюкози4, підвищення рівня тригліцеридів2,5, глюкозурія, підвищення апетиту |
Розвиток або загострення діабету, рідко пов’язаного з кетоацидозом або комою, включаючи деякі летальні випадки11 |
Гіпотермія12 |
|||
|
Порушення з боку нервової системи |
||||||
|
Сонливість |
Запаморочення, акатизія6, Паркінсонізм6, дискінезія6 |
Епілептичні напади, що були в анамнезі або були наявні фактори ризику11, дистонія (включно з окулярним симптомом)11, пізня дискінезія11, амнезія9, дизартрія |
Нейролептичний злоякісний синдром12, синдром відміни7,12 |
|||
|
Порушення з боку системи дихання, органів грудної клітки та медіастинальні порушення |
||||||
|
Кровотеча з носа9 |
||||||
|
Порушення з боку серцевої системи |
||||||
|
Брадикардія, пролонгація інтервалу QTc |
Вентрикулярна тахікардія/фібриляція, раптова смерть11 |
|||||
|
Порушення з боку судинної системи |
||||||
|
Ортостатична гіпотензія10 |
Тромбоемболія (включаючи емболію легеневої артерії та глибокий венозний тромбоз) |
|||||
|
Порушення з боку шлунково-кишкового тракту |
||||||
|
Легкі, короткотривалі антихолінергічні ефекти, включаючи запори та сухість у роті |
Здуття живота9 |
Панкреатити11 |
||||
|
Порушення з боку гепатобіліарної системи |
||||||
|
Транзиторні, асимптоматичні підйоми рівня печінкових трансаміназ АлАТ та АсАТ, особливо на початку лікування, периферичні набряки |
Гепатити (включаючи гепатоцелюлярне, холестатичне або змішане ушкодження печінки)11 |
|||||
|
Порушення з боку шкіри та її похідних |
||||||
|
Висипи |
Реакції світлочутливості, алопеція |
|||||
|
Порушення з боку кістково-м’язової системи та сполучної тканини |
||||||
|
Артралгія9 |
Рабдоміоліз11 |
|||||
|
Порушення з боку нирок та сечовидільної системи |
||||||
|
Нетримання сечі; затримка сечі, затримка сечі, утруднене сечовипускання11 |
||||||
|
Вагітність, післяродовий та перинатальний період |
||||||
|
Синдром відміни у новонароджених |
||||||
|
Порушення з боку репродуктивної системи та молочних залоз |
||||||
|
Еректильна дисфункція у чоловіків; зниження лібідо у жінок та чоловіків |
Аменорея; збільшення грудей; галакторея у жінок; гінекомастія/збільшення грудей у чоловіків |
Пріапізм12 |
||||
|
Загальні розлади та особливості застосування |
||||||
|
Астенія, втомлюваність, набряки, пірексія 10 |
||||||
|
Дослідження |
||||||
|
Підвищення рівня пролактину в плазмі8 |
Підвищення рівня алкалін- фосфатази10, підвищення креатинфосфокінази11, підвищення рівня гаммаглутамілтрансферази10, підвищення рівня сечової кислоти10 |
Підвищення загального білірубіну |
||||
|
Вагітність, післяродовий та перинатальний період |
||||||
|
Частота невідома Синдром відміни у новонароджених |
||||||
1Клінічно значуще збільшення маси тіла спостерігалося у всіх категорій пацієнтів за ІМТ (індекс маси тіла). Після короткочасного лікування (середня тривалість становила 47 днів) збільшення маси тіла на ≥ 7 % спостерігалося дуже часто (22,2 % випадків), ≥ 15 % спостерігалося часто (4,2 % випадків), ≥ 25% спостерігалося нечасто (0,8 % випадків). У пацієнтів, які отримували тривалу терапію (принаймні протягом 48 тижнів), збільшення маси тіла на ≥ 7 %, ≥ 15 %, ≥ 25% спостерігалося дуже часто (у 64,4 %, 31,7 %, 12,3 % випадків відповідно).
2Середні підвищення рівня ліпідів натще (загальний холестерол, ЛПНЩ і тригліцериди) були більш значні у пацієнтів, у яких спочатку не спостерігалося ліпідної дисрегуляції.
3Спостерігалося у пацієнтів з нормальним початковим рівнем натще (< 5,17 ммоль / л), який підвищувався до високого (≥ 6,2 ммоль/л). Дуже часто повідомлялося про різке підвищення рівня загального холестеролу натще (≥ 6,2 ммоль /л).
4Спостерігалося у пацієнтів з нормальним початковим рівнем натще (< 5,56 ммоль / л), який підвищувався до високого (≥ 7 ммоль/л). Дуже часто повідомлялося про різке підвищення рівня глюкози натще (≥ 7 ммоль / л).
5Спостерігалося у пацієнтів з нормальним початковим рівнем натще (<1,69 ммоль / л), який підвищувався до високого (≥ 2,26 ммоль/л). Дуже часто повідомлялося про різке підвищення рівня тригліцеридів натще
(≥ 2,26 ммоль / л).
6Під час клінічних досліджень частота виникнення паркінсонізму і дистонії у пацієнтів, які отримують лікування оланзапіном, була вища, ніж у ході досліджень плацебо, але клінічно незначно. Частота виникнення паркінсонізму, акатизіі і дистонії у пацієнтів, які отримують лікування оланзапіном, була нижча, ніж при застосуванні титрованих доз галоперидолу. Через відсутність інформації про наявність в анамнезі гострих або пізніх екстрапірамідальних рухових порушень не можна встановити, що оланзапін менше спричиню\ пізню дискінезію, та/або інші пізні екстрапірамідальні синдроми.
7У випадку різкого припинення терапії оланзапіном повідомлялося про гострі симптоми: підвищене потовиділення, безсоння, тремор, ажитацію, нудоту і блювання.
8У ході клінічних досліджень (до 12 тижнів) визначено, що концентрація пролактину у плазмі крові перевищувала верхній ліміт норми у 30 % пацієнтів, які застосовували оланзапін. У більшості пацієнтів таке підвищення було помірним і залишалося в межах значень у два рази нижче верхнього рівня норми.
9Побічні реакції визначено в результаті клінічних досліджень в інтегрованій базі даних оланзапіну.
10Оцінка виміряних значень визначена в результаті клінічних досліджень в інтегрованій базі даних оланзапіну.
11Побічні реакції визначено зі спонтанних постмаркетингових звітів з періодичністю, що встановлена на основі інтегрованої бази даних оланзапіну.
12Побічні реакції визначено зі спонтанних постмаркетингових звітів з періодичністю, що оцінена з використанням довірчого інтервалу в верхньому ліміті норми (95 %) основі інтегрованої бази даних оланзапіну.
Вплив при довготривалому застосуванні (не менше 48 тижнів). Відсоток пацієнтів, у яких відзначалися побічні реакції у вигляді клінічно суттєвого підвищення маси тіла, зміни рівня глюкози, загального холестерину/ЛПНЩ/ЛПВЩ або тригліцеридів, постійно збільшувалося. У дорослих пацієнтів, які закінчили 9-12 місячний курс терапії, темп підвищення рівня глюкози в крові натще уповільнився приблизно після 6 місяців лікування.
Побічні дії для окремих групах пацієнтів. У ході клінічних досліджень у пацієнтів літнього віку із деменцією терапія оланзапіном була пов’язана з підвищеним рівнем летальних випадків та цереброваскулярними побічними реакціями порівняно з такими у групі плацебо. Дуже поширеними небажаними ефектами, пов’язаним із застосуванням оланзапіну, у даної групи пацієнтів були порушення ходи та падіння. Часто спостерігалася пневмонія, підвищення температури тіла, летаргія, еритема, зорові галюцинації та нетримання сечі.
У ході клінічних досліджень серед пацієнтів з медикаментозно індукованим (агоніст допаміну) психозом, пов’язаним із хворобою Паркінсона, погіршення паркінсонівської симптоматики та галюцинації відзначалося дуже часто, частіше, ніж у групі плацебо.
У ході одного клінічного дослідження у пацієнтів із біполярною манією в результаті застосування оланзапіну у комбінації з вальпроатом спостерігалася нейтропенія 4,1 %; можливою причиною може бути підвищення рівня вальпроату у плазмі крові.
У результаті застосування оланзапіну з літієм або вальпроатом спостерігалися (≥ 10 %) тремор, сухість у роті, збільшення маси тіла, підвищення апетиту. Також повідомлялося про порушення мовлення. Під час терапії оланзапіном у комбінації з літієм або дивалпроексом спостерігалося збільшення маси тіла ≥ 7 % від ІМТ (індексу маси тіла) у 17,4 % пацієнтів під час інтенсивної терапії (до 6 тижнів). Довготривале лікування оланзапіном (до 12 тижнів) для попередження рецидивів у пацієнтів із біполярними розладами було пов’язано з підвищенням маси тіла ≥ 7 % від ІМТ у 39,9 % пацієнтів.
Діти.
Оланзапін не показаний для лікування дітей та підлітків (віком до 18 років). Клінічні дослідження, які порівнювали застосування оланзапіну у підлітків та дорослих, не проводились.
Нижче подано побічні реакції, що зустрічались частіше у підлітків (віком від 13-17 років), ніж у дорослих, або побічні реакції, що були виявлені тільки під час короткотривалих клінічних досліджень у підлітків. Клінічно значуще збільшення маси тіла (≥ 7 %) частіше спостерігалось у підлітків порівняно з дорослими. Під час довготривалого лікування (не менше 24 тижнів) клінічно значуще збільшення маси тіла було вищим, ніж під час короткотривалого лікування.
Частоту побічних реакцій, зазначених нижче, визначають таким чином: дуже часто (≥ 1/10), часто (≥ 1/100 - < 1/10).
Порушення обміну речовин та розлади травлення.
Дуже часто: збільшення маси тіла13, підвищення рівня тригліцеридів14, підвищення апетиту.
Часто: підвищення рівня холестерину15.
Порушення з боку нервової системи.
Дуже часто: седація (у тому числі гіперсомнія, млявість, сонливість).
Порушення з боку шлунково-кишкового тракту.
Часто: сухість у роті.
Порушення з боку гепатобіліарної системи.
Дуже часто: підвищення рівня печінкових трансаміназ (АлАТ та АсАТ).
Дослідження.
Дуже часто: зниження рівня загального білірубіну, підвищення рівня гаммаглутамілтрансферази, підвищення рівня пролактину в плазмі16.
13Після короткочасного лікування (середня тривалість становила 22 дні) збільшення маси тіла на ≥ 7 % спостерігалося дуже часто (40,6 % випадків), ≥ 15 % спостерігалося часто (7,1 % випадків) та ≥ 25 % (2,5 % випадків). Під час довготривалого лікування (не менше 24 тижнів) у 89,4 % пацієнтів спостерігалося збільшення маси тіла на ≥ 7 %, у 55,3 % – на ≥ 15 % та у 29, 1 % – на ≥ 25 %.
14Спостерігалося у пацієнтів з нормальним початковим рівнем натще (< 1,016 ммоль/л), який підвищувався до високого (≥ 1,467 ммоль/ л), та різке підвищення рівня тригліцеридів натще з початкового рівня (≥ 1,016 - < 1,467 ммоль/л) до високого рівня (≥ 1,467 ммоль/л).
15Спостерігалося у пацієнтів з нормальним початковим рівнем холестеролу натще з початкового рівня (< 4,39 ммоль/л) до високого рівня (≥ 5,17 ммоль/л). Дуже часто повідомлялося про різке підвищення рівня загального холестеролу натще з початкового рівня (≥ 4,39 - < 5,17 ммоль/л) до високого рівня (≥ 5,17 ммоль/л).
16У 47,4 % підлітків спостерігалось підвищення рівня пролактину в плазмі.Інші побічні реакцій, що спостерігалися в ході оцінки клінічних досліджень перорального застосування оланзапіну.
Інші побічні реакцій, що спостерігалися в ході клінічних досліджень перорального застосування оланзапіну.
Порушення з боку нервової системи: нечасто (≥ 0,1 % ) – атаксія, дизартрія.
Дуже рідко повідомлялося про синдром відміни (включаючи діарею, нудоту, блювання).
Із постмаркетингового досвіду повідомлялося про нижчезазначені побічні явища.
Порушення з боку гепатобіліарної системи: дуже рідко (< 0,01%)– жовтяниця.
Порушення з боку шкіри та її похідних: рідко (< 0,1% и > 0,01%) – висипання.
Зміни з боку імунної системи: алергічні реакції, включаючи: дуже рідко (< 0,01%) – анафілактоїдні реакції, ангіоневротичний набряк (< 0,01%), кропив’янка або свербіж.
Інші основні небажані явища і частота їх виникнення, характерна для пацієнтів з біполярною манією, які отримують оланзапін у комбінації з літієм чи вальпроатом.
Дуже часто повідомлялося про тремор (> 10 %). Про порушення мовлення повідомлялося часто (> 1% та <10%).
Інші основні небажані явища і частота їх виникнення, характерна для пацієнтів з індукованим лікарським засобом (агоністом допаміну) психозом, пов'язаним з хворобою Паркінсона.
Дуже часто повідомлялося про галюцинації (> 10 %).
Інші основні небажані явища і частота їх виникнення, характерна для літніх пацієнтів з психозом на тлі деменції.
Дуже часто повідомлялося про порушення ходи (> 10 %).
Термін придатності. 5 років.
Умови зберігання.
Зберігати при температурі не вище 30 °С в оригінальній упаковці у недоступному для дітей місці.
Упаковка.
По 7 таблеток, вкритих плівковою оболонкою, у блістері; по 4 або 8 блістерів у картонній упаковці.
Категорія відпуску. За рецептом.
Виробник.
ЗАТ Фармацевтичний завод ЕГІС/EGIS Pharmaceuticals PLC.
Місцезнаходження виробника та його адреса місця провадження діяльності.
1165, м. Будапешт, вул. Бекеньфелді, 118-120, Угорщина/1165, Budapest, Bokenyfoldi ut., 118-120, Hungary.
Аналоги
Совпадает код ATХ + действующие вещества + форма випуска
| Международное название | Olanzapine |
| Код АТХ | N05AH03 |
| Форма выпуска | таблетки |
- ЗИПРЕКСА® ЗИДИС Каталент ЮК Свіндон Зидис Лімітед (відповідальний за виробництво in-bulk готового лікарського засобу)/Елі Ліллі енд Компані Лімітед (відповідальний за виробництво in-bulk готового лікарського засобу)/Ліллі С.А. (відповідальний за випуск серії готового лік
- ЗИПРЕКСА® ЗИДИС Каталент ЮК Свіндон Зидис Лімітед (відповідальний за виробництво in-bulk готового лікарського засобу)/Елі Ліллі енд Компані Лімітед (відповідальний за виробництво in-bulk готового лікарського засобу)/Ліллі С.А. (відповідальний за випуск серії готового лік
- ЗИПРЕКСА® Ліллі С.А. (виробництво за повним циклом)/Ліллі дель Карібе Інк. (виробництво готової лікарської форми), Іспанія/Пуерто Ріко (США)
- ЗИПРЕКСА® Ліллі С.А. (виробництво за повним циклом)/Ліллі дель Карібе Інк. (виробництво готової лікарської форми), Іспанія/Пуерто Ріко (США)
- ЗОЛАФРЕН Заклад Фармацевтичний Адамед Фарма С.А. (виробник "in bulk", первинного та вторинного пакування)/Паб'яніцький фармацевтичний завод Польфа А.Т. (контроль якості та дозвіл на випуск серії), Польща/Польща
- ЗОЛАФРЕН Заклад Фармацевтичний Адамед Фарма С.А. (виробник "in bulk", первинного та вторинного пакування)/Паб'яніцький фармацевтичний завод Польфа А.Т. (контроль якості та дозвіл на випуск серії), Польща/Польща
- Заласта 10 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта 15 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта 2,5 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта 20 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта 5 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта 7,5 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта Q-Tab 10 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта Q-Tab 15 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта Q-Tab 20 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта Q-Tab 5 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Заласта Q-Tab 7,5 мг КРКА, д.д., Ново место/КРКА, Польща Сп.з.о.о., Словенія/Польща
- Оланкляйн 10 мг Д-р Редді'с Лабораторіс Лтд, Індія
- Оланкляйн 2,5 мг Д-р Редді'с Лабораторіс Лтд, Індія
- Оланкляйн 5 мг Д-р Редді'с Лабораторіс Лтд, Індія
- Парнасан 10 мг ВАТ "Гедеон Ріхтер" (випуск серії)/ТОВ "Гедеон Ріхтер Польща" (контроль якості, дозвіл на випуск серії; виробництво нерозфасованого продукту, первинна упаковка, вторинна упаковка), Угорщина/Польща
- Парнасан 5 мг ВАТ "Гедеон Ріхтер" (випуск серії)/ТОВ "Гедеон Ріхтер Польща" (контроль якості, дозвіл на випуск серії; виробництво нерозфасованого продукту, первинна упаковка, вторинна упаковка), Угорщина/Польща
- Эголанза 10 мг ЗАТ Фармацевтичний завод ЕГІС, Угорщина
- Эголанза 15 мг ЗАТ Фармацевтичний завод ЕГІС, Угорщина
- Эголанза 20 мг ЗАТ Фармацевтичний завод ЕГІС, Угорщина
- Эголанза 7,5 мг ЗАТ Фармацевтичний завод ЕГІС, Угорщина



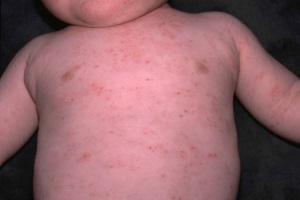 Синдром Віскотта-Олдрича
Синдром Віскотта-Олдрича
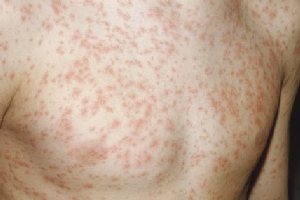 Краснуха
Краснуха
 Инфекционный мононуклеоз
Инфекционный мононуклеоз
 Cистемні прояви цирозу печінки вірусної етіології
Cистемні прояви цирозу печінки вірусної етіології