Оксалиплатин -Эбеве инструкция, аналоги и состав
Склад:
діюча речовина: оксаліплатин (oxaliplatin);
1 флакон містить 50 мг або 100 мг оксаліплатину;
допоміжні речовини: лактози моногідрат.
Лікарська форма. Порошок ліофілізований для приготування розчину для інфузій.
Фармакотерапевтична група. Антинеопластичні засоби. Сполуки платини. Код АТС L01XA03.
Клінічні характеристики.
Показання.
Оксаліплатин застосовується в комбінації з 5-фторурацилом і фоліновою кислотою для:
-
ад'ювантної терапії раку товстого кишечнику стадії ІІІ (С за класифікацією Dukes) після повної резекції первинної пухлини;
-
лікування метастатичного колоректального раку.
Протипоказання.
-
Гіперчутливість до оксаліплатину в анамнезі.
-
Вагітність, годування груддю.
-
Пригнічення функції кісткового мозку до початку першого курсу терапії (кількість нейтрофілів < 2 × 109/л та/або кількість тромбоцитів < 100 × 109/л).
-
Периферична сенсорна нейропатія з функціональними порушеннями до початку першого курсу терапії.
-
Тяжкі порушення функції нирок (кліренс креатиніну < 30 мл/хв).
Спосіб застосування та дози.
Оксаліплатин необхідно вводити лише перед фторпіримідинами (5-фторурацилом)!
Дози для дорослих
Рекомендована доза при ад'ювантній терапії раку товстого кишечнику – 85 мг/м2 поверхні тіла внутрішньовенно кожні 2 тижні, всього 12 курсів (загальна тривалість лікування 6 місяців).
Рекомендована доза при терапії метастатичного колоректального раку – 85 мг/м2 поверхні тіла внутрішньовенно кожні 2 тижні.
Дози коригують залежно від переносимості терапії.
Оксаліплатин застосовують переважно в комбінації з 5-фторурацилом, який вводять шляхом тривалих інфузій.
Дози для хворих з порушеннями функції нирок
Дія оксаліплатину на хворих з тяжкими порушеннями функції нирок не досліджувалася, тому таким пацієнтам препарат протипоказаний. У разі незначних порушень функції нирок або порушень функції нирок середньої тяжкості лікування можна починати у звичайних рекомендованих дозах і коригувати їх залежно від вираженості токсичних ефектів (див. "Особливості застосування").
Дози для хворих з порушеннями функції печінки
Дія оксаліплатину на хворих з тяжкими порушеннями функції печінки досліджена недостатньо. Не відзначено збільшення гострої токсичності при лікуванні оксаліплатином пацієнтів з відхиленнями результатів функціональних печінкових тестів перед початком терапії, тому в таких випадках коригувати дози зазвичай немає потреби.
Дози для літніх пацієнтів
Не відзначено збільшення частоти тяжких токсичних ефектів у пацієнтів віком понад 65 років при монотерапії оксаліплатином або комбінованій терапії оксаліплатином у поєднанні за 5-фторурацилом, тому коригувати дози в таких випадках немає потреби.
Спосіб застосування
-
Оксаліплатин не можна вводити з допомогою інфузійних систем, до складу яких входять алюмінієві частини, або через голки, що містять алюміній.
-
Розчин оксаліплатину з концентрацією 5 мг/мл не можна вводити нерозведеним.
-
Оксаліплатин не можна розчиняти в розчині натрію хлориду або розводити розчином натрію хлориду.
-
Оксаліплатин не можна змішувати з будь-якими іншими лікарськими засобами в одному інфузійному мішку/флаконі або вводити одночасно через одну інфузійну лінію (особливо 5‑фторурацил, лужні лікарські засоби, трометамол і препарати фолінової кислоти, які містять трометамол).
-
Оксаліплатин можна вводити одночасно з фоліновою кислотою через Y-подібний трійник, розміщений безпосередньо перед місцем ін'єкції. Оксаліплатин і фолінову кислоту забороняється змішувати в одному інфузійному мішку/флаконі. Фолінова кислота повинна бути розведена 5% розчином глюкози.
-
Після введення оксаліплатину інфузійну лінію і вену промивають 5% розчином глюкози.
Розчинення ліофілізованого порошку
У флакон по 50 мг додають 10 мл води для ін'єкцій або 5% розчину глюкози для одержання розчину з концентрацією оксаліплатину 5 мг/мл.
У флакон по 100 мг додають 20 мл води для ін'єкцій або 5% розчину глюкози для одержання розчину з концентрацією оксаліплатину 5 мг/мл.
Приготовлений розчин перевіряють візуально. Можна використовувати лише прозорий розчин без механічних включень. Розчин оксаліплатину з концентрацією 5 мг/мл негайно розводять 5% розчином глюкози. Дозволяється лише одноразовий відбір препарату з флакону. Невикористані залишки розчину знищують.
Приготування розчину для інфузій
Потрібну кількість розчину оксаліплатину з концентрацією 5 мг/мл розводять 250-500 мл 5% розчину глюкози. Концентрація розчину для інфузій повинна бути не меншою за 0,2 мг/мл. Приготовлений розчин перевіряють візуально. Можна використовувати лише прозорий розчин без механічних включень. Розведений розчин для інфузій є фізично і хімічно стабільним протягом 24 год у разі зберігання при температурі 2-8°C. З мікробіологічної точки зору розведений розчин слід використовувати негайно.
Введення
Застосування оксаліплатину не вимагає попередньої гіпергідратації.
Розчин для інфузій вводять у периферичні або центральні вени протягом 2-6 годин. У разі екстравазації інфузію негайно припиняють і призначають місцеве симптоматичне лікування. При комбінованому застосуванні у поєднанні з 5-фторурацилом оксаліплатин необхідно вводити лише перед 5‑фторурацилом.
Інструкції персоналу
Враховуючи токсичність оксаліплатину, рекомендуються нижченаведені запобіжні заходи:
-
Персонал повинен мати відповідну кваліфікацію і бути поінформованим щодо техніки роботи з препаратом.
-
При маніпуляціях з препаратом слід додержуватися правил роботи з цитостатиками.
-
Вагітні медичні працівники не повинні працювати з препаратом.
-
При роботі з препаратом персонал повинен користуватися захисним одягом: халатами, шапочками, масками, окулярами і одноразовими рукавичками.
-
Для маніпуляцій з препаратом необхідно виділити спеціальне місце, де заборонено курити, їсти та пити. Робочі поверхні повинні бути закриті одноразовими аркушами абсорбуючого паперу із захисним плівковим покриттям зі зворотного боку.
-
Залишки препарату, всі речі та матеріали, які використовувалися при розчиненні, розведенні і введенні розчинів оксаліплатину, а також прибиранні (включаючи рукавички), повинні складатися у спеціальні контейнери або високоміцні мішки для токсичних відходів і знищуватися у відповідності зі стандартною лікарняною процедурою утилізації відходів цитотоксичних речовин згідно з діючими нормативними актами щодо знищення небезпечних відходів.
-
Необхідно з обережністю прибирати блювоту та екскрети пацієнтів.
-
При випадковому потраплянні ліофілізованого порошку або розчинів оксаліплатину на шкіру або слизові оболонки їх слід негайно промити великою кількістю води.
Побічні реакції.
При комбінованій терапії оксаліплатином і 5-фторурацилом/фоліновою кислотою найчастіше відзначаються побічні ефекти з боку травного тракту (діарея, нудота, блювання і запалення слизових оболонок), з боку системи кровотворення (нейтропенія, тромбоцитопенія) і з боку нервової системи (гостра і кумулятивна периферична сенсорна нейропатія). Загалом частота і тяжкість небажаних побічних ефектів при комбінованій терапії оксаліплатином і 5‑фторурацилом/фоліновою кислотою вище, ніж при терапії лише 5-фторурацилом/ фоліновою кислотою.
З боку системи кровотворення
Дуже часті (> 10%). Анемія, нейтропенія, тромбоцитопенія, лейкопенія, лімфопенія.
Часті (>1% – <10%). Фебрильна нейтропенія/нейтропенічний сепсис (нейтропенія 3-4 ступеня з документованими інфекціями).
З боку травного тракту
Дуже часті (> 10%). Діарея, нудота, блювання, стоматит/запалення слизових оболонок, абдомінальний біль, запор, анорексія.
Часті (>1% – <10%). Диспепсія, гастроезофагеальний рефлюкс, гикавка.
Нечасті (>0,1% – <1%). Непрохідність кишечнику, обструкція кишечнику.
Поодинокі (<0,1%). Коліт (зокрема коліт і діарея, спричинені Clostridium difficile), панкреатит.
З боку автономної нервової системи
Часті (>1% – <10%). Припливи.
З боку центральної і периферичної нервової системи
Дуже часті (> 10%). Периферична сенсорна нейропатія, головний біль, сенсорні порушення.
Часті (>1% – <10%). Запаморочення, моторний неврит, менінгізм.
Поодинокі (<0,1%). Дизартрія, втрата глибоких сухожильних рефлексів і симптом Лермітта.
Метаболічні розлади
Часті (>1% – <10%). Дегідратація.
Нечасті (>0,1% – <1%). Метаболічний ацидоз.
З боку м'язово-кісткової системи
Дуже часті (> 10%). Біль у спині.
Часті (>1% – <10%). Артралгія, біль у кістяку.
З боку системи згортання крові
Дуже часті (> 10%). Носова кровотеча.
Часті (>1% – <10%). Кровотечі, гематурія, тромбофлебіт глибоких вен, емболія легеневої артерії, кровотеча з прямої кишки.
Психіатричні ефекти
Часті (>1% – <10%). Депресія, безсоння.
Нечасті (>0,1% – <1%). Нервозність, підвищена збудливість.
З боку імунної системи
Дуже часті (> 10%). Інфекції.
З боку дихальної системи
Дуже часті (> 10%). Задишка, кашель.
Часті (>1% – <10%). Риніт, інфекції верхніх дихальних шляхів.
Поодинокі (<0,1%). Інтерстиціальна хвороба легенів, фіброз легенів.
З боку шкіри та її придатків
Дуже часті (> 10%). Дерматологічні реакції, алопеція.
Часті (>1% – <10%). Ексфоліація шкіри (синдром рук і ніг), еритематозні висипи, шкірні висипи, підвищена пітливість, зміни нігтів.
З боку органів чуття
Дуже часті (> 10%). Порушення смаку.
Часті (>1% – <10%). Кон'юнктивіт, порушення зору.
Нечасті (>0,1% – <1%). Ототоксичні ефекти.
Поодинокі (<0,1%). Глухота, транзиторне зниження гостроти зору, порушення поля зору, неврит зорового нерва.
З боку системи сечовиділення
Часті (>1% – <10%). Дизурія, аномальна частота сечовипускання.
Загального характеру
Дуже часті (> 10%). Пропасниця внаслідок інфекцій (з фебрильною нейтропенією або без неї) або спричинена імунологічним механізмом; утома; алергічні реакції (зокрема шкірні висипання, кропив'янка, кон'юнктивіт, риніт) та анафілактичні реакції (зокрема бронхоспазм, ангіоневротичний набряк, гіпотензія та анафілактичний шок); астенія, біль, збільшення маси тіла (при ад'ювантній терапії раку товстого кишечнику).
Часті (>1% – <10%). Біль у грудях, зниження маси тіла (при лікуванні метастатичного колоректального раку).
Поодинокі (<0,1%). Імуноалергічна тромбоцитопенія, гемолітична анемія.
Місцеві реакції
Дуже часті (> 10%). Реакції в місцях ін'єкцій (біль, запалення).
Лабораторні показники
Дуже часті (> 10%). Підвищення в крові рівня лужної фосфатази, підвищення рівня білірубіну, відхилення рівня глюкози, підвищення рівня лактатдегідрогенази, гіпокаліємія, підвищення активності печінкових ферментів АЛТ і АСТ, відхилення рівня натрію.
Часті (>1% – <10%). Підвищення рівня креатиніну.
Дозолімітуючим фактором при лікуванні оксаліплатином є нейротоксичність. Розвивається сенсорна периферична нейропатія, яка характеризується дизестезією та/або парестезією кінцівок з судомами або без них, що часто спричиняються холодом. Ці симптоми відзначаються майже у 95% пацієнтів. Тривалість цих симптомів, які зазвичай регресують між курсами лікування, зростає зі збільшенням кількості курсів.
Поява болю та/або функціональних порушень, залежно від тривалості симптомів, є показанням до корекції доз або навіть відміни препарату.
Функціональні порушення, зокрема утруднення виконання точних рухів, є можливим наслідком сенсорних порушень. Ризик появи стійких симптомів становить приблизно 10% при кумулятивній дозі 850 мг/м2 поверхні тіла (10 курсів) і приблизно 20% при кумулятивній дозі 1020 мг/м2 поверхні тіла (12 курсів).
В більшості випадків неврологічні симптоми регресують або повністю зникають після припинення лікування. Через 6 місяців після закінчення ад'ювантної терапії раку товстого кишечнику у 87% пацієнтів неврологічні симптоми не спостерігалися або були слабкими. Через 3 роки приблизно у 3% пацієнтів були наявні стійкі локалізовані парестезії середньої тяжкості (2,3%) або парестезії, які заважали функціональній діяльності (0,5%).
Повідомлялося про розвиток гострих нейросенсорних симптомів, які з'являлися протягом декількох годин після введення оксаліплатину, часто – під впливом холоду. Вони можуть включати транзиторну парестезію, дизестезію і гіпестезію або гострий синдром ларингофарингеальної дизестезії. Цей синдром, частота якого становить 1-2%, характеризується суб'єктивним відчуттям дисфагії або диспное без об'єктивних клінічних ознак респіраторного дистресу (без ціанозу або гіпоксії), або лагингоспазмом, або бронхоспазмом (без стридорозного дихання). Також можливі спазм жувальних м'язів, дизестезія язика, дизартрія і відчуття тиску в грудній клітці. Хоча в таких випадках застосовували антигістамінні і бронхорозширювальні препарати, симптоми швидко минають навіть без усякого втручання. Збільшення тривалості інфузії допомагає зменшити частоту проявів цього синдрому.
Передозування.
Специфічний антидот оксаліплатину невідомий. У разі передозування можна очікувати більш тяжких побічних ефектів. Необхідний регулярний моніторинг гематологічних показників. Лікування симптоматичне.
Застосування у період вагітності або годування груддю.
Безпечність застосування оксаліплатину в період вагітності не досліджувалася. Доклінічні дані свідчать про те, що оксаліплатин в терапевтичних дозах може чинити ембріолетальну та/або тератогенну дію на плід, тому препарат не рекомендується застосовувати в період вагітності. Призначення препарату можливе тільки після ретельного зважування користі і ризику, а також після інформування пацієнтки про ризик для плоду і за умови її згоди.
Екскреція оксаліплатину з жіночим молоком не вивчалася. В період лікування оксаліплатином годування груддю необхідно припинити.
Діти.
Безпека й ефективність лікування оксаліплатином досліджувалася лише на дорослих пацієнтах, специфічна інформація щодо лікування дітей відсутня.
Особливості застосування.
Лікування оксаліплатином повинно здійснюватися лише в спеціалізованих онкологічних відділеннях під наглядом досвідчених лікарів-онкологів.
Враховуючи обмежену інформацію щодо лікування оксаліплатином хворих з порушеннями функції нирок середньої тяжкості, призначати препарат в таких випадках можна лише після ретельного зважування користі і ризику. При лікуванні оксаліплатином хворих з дисфункцією нирок необхідний регулярний контроль функції нирок і коригування доз залежно від токсичних ефектів.
Пацієнти з алергічними реакціями на сполуки платини в анамнезі повинні перебувати під пильним наглядом. У разі анафілактичної/анафілактоїдної реакції на оксаліплатин інфузію препарату негайно припиняють і призначають відповідне симптоматичне лікування. Повторне призначення оксаліплатину в таких випадках протипоказане.
Необхідно пильно контролювати нейротоксичну дію оксаліплатину, особливо у разі комбінованого застосування з іншими нейротоксичними препаратами. Неврологічні обстеження необхідно проводити перед кожною інфузією оксаліплатину і потім періодично.
Якщо під час або протягом декількох годин після двогодинної інфузії оксаліплатину в пацієнта розвивається ларингофарингеальна дизестезія, тривалість наступної інфузії препарату має становити 6 годин.
При появі симптомів нейротоксичної дії (парестезія, дизестезія) наступні дози оксаліплатину необхідно знижувати залежно від тривалості і тяжкості симптомів:
-
Якщо симптоми спостерігаються більше 7 днів і турбують пацієнта, наступну дозу оксаліплатину знижують з 85 до 65 мг/м2 поверхні тіла (при лікуванні метастатичного колоректального раку) або до 75 мг/м2 поверхні тіла (при ад'ювантній терапії раку товстого кишечнику).
-
Якщо парестезія без функціональних порушень спостерігається до початку наступного курсу терапії, наступну дозу оксаліплатину знижують з 85 мг/м2 до 65 мг/м2 поверхні тіла (при лікуванні метастатичного колоректального раку) або до 75 мг/м2 поверхні тіла (при ад'ювантній терапії раку товстого кишечнику).
-
Якщо парестезія з функціональними порушеннями спостерігається до початку наступного курсу терапії, оксаліплатин необхідно відмінити.
-
У разі зникнення симптомів нейротоксичної дії після відміни препарату можна розглянути доцільність відновлення терапії.
Пацієнтів необхідно інформувати про те, що симптоми периферичної сенсорної нейропатії можуть зберігатися після закінчення лікування оксаліплатином (локалізовані парестезії середньої тяжкості або парестезії, які заважають функціональній діяльності, можуть проявлятися до трьох років після закінчення ад'ювантної терапії оксаліплатином).
Профілактичне та/або терапевтичне застосування антиеметиків може допомогти послабити шлунково-кишкові токсичні ефекти (нудоту і блювання). Тяжка діарея/блювання можуть спричинити дегідратацію, паралітичну непрохідність кишечнику, обструкцію шлунково-кишкового тракту, гіпокаліємію, метаболічний ацидоз і порушення функції нирок, особливо при комбінованому застосуванні оксаліплатину і 5-фторурацилу.
У разі гематологічних токсичних ефектів (кількість нейтрофілів < 1,5 × 109/л та/або кількість тромбоцитів < 50 × 109/л) наступний курс терапії оксаліплатином відстрочують до відновлення гематологічних показників. До початку лікування і перед кожним курсом терапії необхідно проводити повний аналіз крові з диференціацією лейкоцитів.
Якщо у пацієнта розвивається запалення слизових оболонок/стоматит з нейтропенією або без неї, наступний курс лікування відстрочується до зменшення тяжкості запалення слизових оболонок/стоматиту до ступеня 1 або нижче та/або збільшення кількості нейтрофілів до 1,5 × 109/л.
Пацієнти повинні бути поінформовані про ризик виникнення діареї/блювання, запалення слизових оболонок/стоматиту та нейтропенії і про необхідність негайно звертатися до лікаря при появі відповідних симптомів.
Якщо оксаліплатин застосовується у поєднанні з 5-фторурацилом (з фоліновою кислотою або без неї), дози 5-фторурацилу коригують залежно від токсичних ефектів за звичайною схемою.
У разі діареї IV ступеня, нейтропенії III-IV ступеня (кількість нейтрофілів < 1,0 × 109/л) або тромбоцитопенії III-IV ступеня (кількість тромбоцитів < 50 × 109/л) дози оксаліплатину знижують з 85 мг/м2 до 65 мг/м2 поверхні тіла (при лікуванні метастатичного колоректального раку) або до 75 мг/м2 поверхні тіла (при ад'ювантній терапії раку товстого кишечнику), а також знижують дози 5-фторурацилу.
У разі непояснених симптомів з боку дихальної системи (таких як непродуктивний кашель, задишка, крепітація або інфільтрати на рентгенограмі легенів) оксаліплатин необхідно відмінити до проведення пульмонологічного обстеження з метою виключення інтерстиціальної хвороби легенів.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами
Вплив оксаліплатину на швидкість реакції при керуванні автотранспортом або іншими механізмами не досліджувався, однак потенційно можливі побічні ефекти (такі як запаморочення, нудота, блювання та неврологічні симптоми) можуть певною мірою впливати на здатність керувати автотранспортом або іншими механізмами.
Взаємодія з іншими лікарськими засобами та інші форми взаємодій.
Одноразове введення оксаліплатину в дозі 85 мг/м2 поверхні тіла безпосередньо перед введенням 5-фторурацилу не впливає на експозицію 5-фторурацилу.
Дослідження in vitro не виявили значного витіснення оксаліплатину, зв'язаного з білками плазми крові, при комбінованому застосуванні з такими препаратами, як еритроміцин, саліцилати, гранісетрон, паклітаксел і натрію вальпроат.
Фармакологічні властивості.
Фармакодинаміка.
Антинеопластичний агент оксаліплатин (цис-[оксалато(транс-l-1,2-діаміноциклогексан) платина]) належить до нового класу сполук платини, в яких атом платини утворює комплекс с 1,2‑діаміноциклогексаном (DACH) і оксалатною групою. Оксаліплатин є енантіомером.
Оксаліплатин виявляє цитотоксичну дію in vitro і протипухлинну дію in vivo щодо широкого спектру тест-систем, зокрема моделей колоректального раку людини. Була продемонстрована активність оксаліплатину in vitro та in vivo щодо різних моделей раку, резистентних до цисплатину.
При комбінованому застосуванні оксаліплатину і 5-фторурацилу in vitro та in vivo спостерігається синергічний цитотоксичний ефект.
Механізм дії оксаліплатину остаточно не з'ясований, однак дослідження показали, що водні деривати, які утворюються при біотрансформації оксаліплатину, взаємодіють з ДНК і спричинюють формування міжниткових і внутрішньониткових зшивок у ДНК, внаслідок чого порушується синтез ДНК і спостерігаються цитотоксичний і протипухлинний ефекти.
Фармакокінетика.
Фармакокінетика окремих активних метаболітів не досліджувалася. Фармакокінетичні показники для ультрафільтрованої платини (суміші всіх незв'язаних, активних і неактивних сполук платини) після двогодинних інфузій оксаліплатину у дозі 130 мг/м2 поверхні тіла кожні 3 тижні (1-5 курсів) або у дозі 85 мг/м2 поверхні тіла кожні 2 тижні (1-3 курси) наведені у таблиці.
|
Доза |
Cmax (мкг/мл) |
ПФК0-48 (мкг·год/мл) |
ПФК (мкг·год/мл) |
t1/2α (год) |
t1/2β (год) |
t1/2γ (год) |
Vss (л) |
CL (л/год) |
|
85 мг/м2 |
||||||||
|
Середні показники |
0,814 |
4,19 |
4,68 |
0,43 |
16,8 |
391 |
440 |
17,4 |
|
Стандартне відхилення |
0,193 |
0,647 |
1,40 |
0,35 |
5,74 |
406 |
199 |
6,35 |
|
130 мг/м2 |
||||||||
|
Середні показники |
1,21 |
8,20 |
11,9 |
0,28 |
16,3 |
273 |
582 |
10,1 |
|
Стандартне відхилення |
0,10 |
2,40 |
4,60 |
0,06 |
2,90 |
19,0 |
261 |
3,07 |
В кінці двогодинної інфузії 15% введеної платини перебуває в системному кровообігу, а 85% швидко розподіляється у тканинах або виводиться із сечею. Внаслідок необоротного зв'язування з еритроцитами і альбуміном плазми періоди напіввиведення платини в цих сполуках близькі до часу природного оновлення еритроцитів і альбуміну плазми крові. При введенні оксаліплатину кожні 2 тижні у дозі 85 мг/м2 поверхні тіла або кожні 3 тижні у дозі 130 мг/м2 поверхні тіла кумуляції платини в ультрафільтраті плазми крові не спостерігається, а рівноважний стан досягається вже після першого курсу терапії. Інтер- та інтрасуб'єктна варіабельність фармакокінетичних показників загалом невелика.
Біотрансформація in vitro вважається результатом безферментної деградації. Немає ознак цитохром Р450 опосередкованого метаболізму діаміноциклогексанового кільця.
В організмі людини оксаліплатин інтенсивно біотрансформується. Після закінчення двогодинної інфузії препарату незмінений оксаліплатин вже не виявляється в ультрафільтраті плазми крові. В системному кровообігу були ідентифіковані декілька цитотоксичних продуктів біотрансформації оксаліплатину, зокрема, монохлор-, дихлор- і діакво-DACH сполуки платини. Пізніше також виявляються неактивні кон'югати платини.
Платина екскретується переважно із сечею (за 5 діб 54% дози виводиться із сечею і < 3% – з фекаліями). Більшість платини виводиться протягом 48 годин після введення препарату.
У хворих з порушеннями функції нирок кліренс платини значно нижчий, ніж у пацієнтів без таких порушень (9,95 ± 1,91 л/год порівняно з 17,6 ± 2,18 л/год). Окрім того, у них статистично значимо нижчий об'єм розподілу (241 ± 36,1 л порівняно з 330 ± 40,9 л). Кліренс платини у пацієнтів з тяжкими порушеннями функції нирок не досліджувався.
Фармацевтичні характеристики.
Основні фізико-хімічні властивості: білий порошок або маса.
Несумісність.
-
Оксаліплатин не можна вводити разом з лужними лікарськими засобами (зокрема 5‑фторурацилом, трометамолом і препаратами фолінової кислоти, які містять трометамол).
-
Оксаліплатин не можна розчиняти в розчині натрію хлориду або розводити розчином натрію хлориду.
-
Оксаліплатин не можна змішувати з іншими лікарськими засобами в одному інфузійному мішку/флаконі або одній інфузійній лінії (інструкції щодо одночасного введення фолінової кислоти наведені в розділі "Спосіб застосування").
-
Оксаліплатин не можна вводити з допомогою інфузійних систем, до складу яких входять алюмінієві частини, або через голки, що містять алюміній.
Термін придатності.
Лікарський препарат (порошок ліофілізований для приготування розчину для інфузій) в оригінальній упаковці – 2 роки.
Розчин з концентрацією оксаліплатину 5 мг/мл, приготований в оригінальному флаконі – з мікробіологічної і хімічної точок зору повинен бути використаний негайно.
Розведений розчин для інфузій є фізично і хімічно стабільним протягом 24 год у разі зберігання при температурі 2-8°C. З мікробіологічної точки зору розведений розчин слід використовувати негайно. Якщо розчин для інфузій не використовується відразу ж, за терміном і умовами його зберігання повинна стежити відповідальна особа. Період зберігання розчину не повинен перевищувати 24 год при температурі 2-8°C.
Умови зберігання.
Зберігати у недоступному для дітей місці при температурі не вище 25°C.



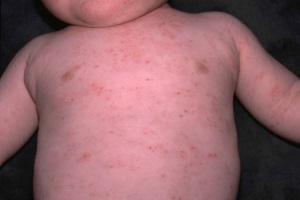 Синдром Віскотта-Олдрича
Синдром Віскотта-Олдрича
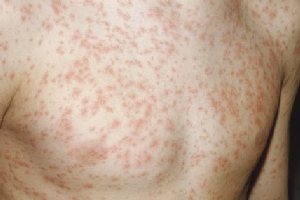 Краснуха
Краснуха
 Инфекционный мононуклеоз
Инфекционный мононуклеоз
 Cистемні прояви цирозу печінки вірусної етіології
Cистемні прояви цирозу печінки вірусної етіології