- Головна
- /
- Статті
- /
- Ендокринологія. Цукровий діабет
- /
- Гіпотиреоз
Гіпотиреоз

Гіпотиреоз – синдром, що розвивається в результаті патологічного зниження функціональної активності щитоподібної залози. При цьому спостерігається різке зниження рівня тиреоїдних гормонів та підвищення рівня тиреотропіну в сироватці крові.
МКХ-10 Е03.0, Е03.1
Общая информация
Гіпотиреоз відноситься до найпоширенішої патології щитоподібної залози у дітей. Гіпотиреоз у дітей може бути вродженим і набутим. Вроджений гіпотиреоз (ВГ) належить до числа доволі поширених і найтяжчих захворювань ЩЗ, що спостерігаються в педіатричній ендокринології. Середня частота ВГ – 1 на 3-4 тис. новонароджених. В 2006 р. в Україні було зареєстровано 1398 дітей віком від 0 до 14 років (20,7 на 100 тис. населення), а кількість вперше виявлених пацієнтів склало 308 (4,6 на 100 тис. населення). Внаслідок незначних клінічних проявів у перші місяці життя ця хвороба нерідко своєчасно не діагностується, а спричинені нею порушення, насамперед розумового розвитку, є найчастіше незворотними. ВГ є однією з основних причин кретинізму, тобто незворотних змін у нервовій та кістковій системі, й затримки росту дитини. ВГ є гетерогенним синдромом і в його етіопатогенезі беруть участь багато різних механізмів, гіпотиреоз може бути як постійним, так і транзиторним.
Постійний гіпотиреоз: первинний гіпотиреоз (пов’язаний з тиреоїдною патологією); тиреоїдний дизгенез: аплазія, ектопія, гіпоплазія ЩЗ; вроджені порушення біосинтезу тиреоїдних гормонів, пов’язані з екстратиреоїдними аномаліями; периферична резистентність до тиреоїдних гормонів.
Транзиторний гіпотиреоз виникає внаслідок прийому йоду або антитиреоїдних препаратів вагітною матір’ю, проникнення крізь плаценту материнських антитіл, які блокують рецептори тиреотропного гормону плоду при аутоімунному тиреоїдиті, недоношеності дитини та дефіциті йоду.
Найчастішими причинами розвитку постійного ВГ є дизгенез (80-85%), дизгормоногенез (10-15%), гіпоталамо-гіпофізарні порушення (<5%) ЩЗ тощо. Етіологія тиреоїдного дизгенезу залишається невідомою. Наявність генетичного дефекту підтверджують такі чинники, як переважання жіночої статі над чоловічою серед дітей з ВГ, наявність інших тиреоїдних порушень у родині хворого на ВГ, поширеність серед близнят і близьких родичів, зв’язок між ВГ та високою частотою появи HLA типів Aw24 або Bw44. Гормональні порушення за різних форм ВГ відрізняються за ступенем тяжкості. Найбільший ступінь тиреоїдної недостатності спостерігається у разі дизембріогенезу ЩЗ, а саме – при її аплазії та дистопії, а також за таких варіантів дизгормоногенезу, як дефект синтезу тиреоїдного гормону. Найменш тяжкі гормональні порушення фіксуються у випадку дефектів тиреопероксидази і синтезу аномального тиреоїдного гормону. В етіології транзиторного порушення функції ЩЗ велике значення має кількість споживання йоду. Дефіцит його є найчастішою причиною ВГ і розумової відсталості.
Провідну роль у розвитку гіпофункції ЩЗ у дітей відіграють також чинники, не пов’язані із забезпеченням плоду і новонародженого йодом, зокрема вплив малих доз іонізуючої радіації, а також інші зобогенні чинники. Відзначено, що у районах з радіаційним забрудненням середня концентрація ТТГ у крові новонароджених вірогідно вища, ніж у дітей із «чистої» місцевості.
Тиреоїдні гормони на етапі внутрішньоутробного розвитку є важливими регуляторами формування і дозрівання головного мозку плода. У І триместрі вагітності повноцінне анатомо-морфологічне закладання ЦНС забезпечують гормони материнської щитоподібної залози, а наступний фетальний розвиток тканини мозку і мієлінізація компонентів міжнейрональних зв’язків залежить від активності щитоподібної залози плоду. Важливу роль у цих процесах відіграє достатнє забезпечення організму фізіологічними дозами йоду. Терміни диференціювання головного мозку чітко обмежені, тому навіть короткий період тиреоїдної недостатності негативно впливає на розвиток ЦНС, призводячи до змін у нервово-психічній сфері.
Крім впливу на закладання і розвиток нервової системи тиреоїдні гормони відіграють також важливу роль у регуляції гомеостазу в період новонародженості, різнобічно впливають на процеси метаболізму, забезпечують тривалу адаптацію до конкретних умов існування. Не менш важливою дією тиреоїдних гормонів у дитячому віці є їх анаболічний ефект. Йодотироніни регулюють не стільки лінійний ріст, скільки процеси диференціювання тканин.
При народженні та у перші 30 хв після пологів у новонароджених унаслідок фізіологічного стресу спостерігається значне зростання вмісту ТТГ у крові – до 70 мОД/л. До кінця 1-2 доби рівень ТТГ падає до початкового (10 мОД/л), а в наступні 3-6 діб життя фіксують поступове зниження концентрації ТТГ у крові й тенденцію до стабілізації його секреції. Якщо високий рівень ТТГ (50-100 мОД/л) зберігається впродовж першого тижня життя, це свідчить про можливий вроджений гіпотиреоз. Вміст вільного Т4 також підвищується у першу добу життя до максимуму, потім знижується на 3 добу, після чого впродовж перших 4 тижнів наростає. Остаточно співвідношення між гормонами ЩЗ встановлюється до 1,5-місячного віку.
Нетривале порушення адаптації гіпофізарно-тиреоїдної системи в новонароджених у постнатальний період, що виявляється клінічними і біохімічними ознаками гіпотиреоїдного стану, розглядається як неонатальний транзиторний гіпотиреоз. Клінічні симптоми транзиторного гіпотиреозу неспецифічні: в’ялість, мармуровість, пастозність шкірних покривів, поганий апетит, зригування, схильність до закрепів, тривала жовтяниця, м’язова гіпотонія, анемія. При гормональному дослідженні виявляють зниження Т4 і/або Т3. Підвищення рівня ТТГ спостерігається не завжди і воно не таке значне, як при ВГ. При цьому рівні Т4 та ТТГ у пуповинній крові нормальні. Обстеження рекомендується проводити не раніше 5 доби життя у доношених і 7-14 доби у недоношених дітей. Поширення транзиторного гіпотиреозу у новонароджених коливається від 1 до 14%.
Встановлено, що перенесений у неонатальному періоді транзиторний гіпотиреоз несприятливо впливає на наступний фізичний, нервово-психічний, мовний розвиток дітей та стан їх здоров’я на першому році життя й у шкільному віці. У більшості новонароджених функція ЩЗ відновлюється до кінця першого місяця життя.
Етіологія
Вроджений гіпотиреоз виникає внаслідок різних причин. Найчастішими причинами виникнення вродженого гіпотиреозу є: порушення морфологічного розвитку щитоподібної залози (повна або часткова її відсутність, ектопія), внутрішньоутробне ушкодження щитоподібної залози, генетично зумовлене порушення біосинтезу тиреоїдних гормонів.
Порушення біосинтезу тиреоїдних гормонів призводить до підвищення виділення тиреотропіну (ТТГ) гіпофізом та збільшення щитоподібної залози.
Особлива форма дефекту перетворення неорганічного йоду на органічний – синдром Пендреда, що характеризується збільшенням щитоподібної залози, глухотою (або недочуванням) і розладами вестибулярної функції. Успадковування відбувається за аутосомно-рецесивним типом.
Можливі причини розвитку набутого гіпотиреозу у дітей наступні: хірургічне втручання на щитоподібній залозі (повне або часткове її видалення); безконтрольне застосування протягом тривалого часу тиреостатичних препаратів або препаратів неорганічного йоду; запальні процеси та аутоімунні порушення в щитоподібній залозі; недостатнє надходження в організм дитини різних мікроелементів, передусім йоду, з водою та харчовими продуктами. Гіпотиреоз може розвинутися після впливу на щитоподібну залозу радіоактивного йоду.
Патогенез
В основі патогенезу всіх форм гіпотиреозу лежить зниження рівня тиреоїдних гормонів у крові.
Патогенез первинного гіпотиреозу визначається відсутністю, недорозвиненістю або ушкодженням власне тиреоїдної тканини, що не спроможна синтезувати достатню кількість тиреоїдних гормонів.
Розвиток вторинного гіпотиреозу спричинений недостатньою продукцією тиреотропіну в гіпофізі.
У патогенезі третинного гіпотиреозу провідне місце посідає порушення вироблення тиреоліберину гіпоталамусом.
Гіпотиреоз може розвиватися і внаслідок резистентності периферичних тканин до дії тиреоїдних гормонів. Дефіцит тиреоїдних гормонів призводить до значних порушень процесів обміну речовин в організмі.
Клиническая картина
Клінічні прояви гіпотиреозу у дітей залежать від віку, коли виникла недостатність функції щитоподібної залози, ступеня тиреоїдної недостатності й тривалості захворювання.
На відміну від дорослих, у дітей на перший план виходить затримка фізичного, розумового та статевого розвитку. Вроджений гіпотиреоз проявляється в перші дні та місяці життя дитини.
Захворювання запідозрюється за таких умов: переношена вагітність (понад 42 тижні), маса тіла під час народження більша за 4000 г, набряклість, здуття живота, схильність до закрепів, пупова грижа, пізнє відпадання пупового канатику, затяжна жовтяниця (тривалість якої може досягати 5-6 міс.). Дитина незвично спокійна, сонлива, рідко кричить, тембр голосу – низький. Шкіра суха, стопи й кисті холодні, язик не вміщається в роті. Часто спостерігаються різні респіраторні симптоми (шумне дихання, що нагадує стридор, утруднене носове дихання, схильність до респіраторних захворювань, напади ціанозу, можливий також типовий дихальний дистрес-синдром). Відзначається уповільнена реакція на больові подразники, гіпестезія, тривала гіпертонія м’язів, симптом Керніга.
Дуже характерні симптоми ураження ЦНС у вигляді сповільнення психічної діяльності, загальмованості, затримки розвитку головного мозку.
Якщо захворювання залишається нерозпізнаним, то через 5-6 міс. виявляють класичну картину гіпотиреозу: затримку психофізичного розвитку, функціональні зміни практично всіх внутрішніх органів, трофічні зміни шкіри та її придатків. Важливим симптомом є порушення термінів та порядку прорізування зубів (як молочних, так і постійних). Закриття великого тім’ячка затримується до 8-10-місячного віку. Ходити діти починають пізно. Згодом спостерігається відставання в рості, при цьому пропорції скелета залишаються інфантильними й наближаються до хондродистрофічних. Порушується розвиток скелету обличчя – перенісся широке, пласке, ніс короткий, очні ямки широко розставлені. Внаслідок браку тироксину, що впливає на процес скостеніння хряща, затримується поява ядер скостеніння скелету. Кістковий вік дитини різко відстає від паспортного. Для тиреоїдного нанізму характерно, що осифікація починається з численних неправильних фокусів, розкиданих по всій зоні зміненого хряща.
Постійний клінічний симптом гіпотиреозу – виражений слизовий набряк (мікседема). Внаслідок затримки води в організмі хвора дитина має надлишкову масу тіла. Шкіра суха, лущиться, бліда, із жовтуватим відтінком. Чоло та повіки набряклі, нависають, очні щілини вузькі, риси обличчя згладжені. Язик набряклий, не вміщається в роті. У надключичній ділянці, на тильному боці стоп і кистей утворюються підвищення у вигляді подушечок.
Основною причиною розвитку слизового набряку є порушення обміну глікопротеїдів, вуглеводні компоненти яких виявлені в набряковій речовині – муцині. Муцин виявляють і в інтерстиціальній тканині серця, м’язів, у нервовій системі, шкірі.
Волосся стає сухим, ламким, рідким. Потовиділення різко знижене. Часті симптоми гіпотиреозу – зміни функціонального стану скелетних м’язів (діти швидко втомлюються, стають млявими). З’являється м’язова гіпотонія, характерна постава з вираженим поперековим лордозом, виступаючими сідницями.
При гіпотиреозі страждають також інші органи й системи дитини. Порушується функція печінки (процес утворення вітаміну А з каротину, виділення білірубіну тощо); знижується рухова активність кишок, що призводить до стійких закрепів і метеоризму. Відзначається виражена брадикардія, кардіомегалія, глухість серцевих тонів, зниження АТ. Скорочувальна функція міокарду порушується за типом гіподинамії. Знижується фільтраційна та секреторна здатність ниркових канальців.
Виявляють анемію (найчастіше – залізодефіцитну) та еозинофілію. Зниження функції ЩЗ спричиняє затримку статевого розвитку; виникають гіпоплазія та дис-функція статевих залоз.
При гіпотиреозі фіксують рентгенологічні зміни черепа: у 50% дітей спостерігається брахіцефалія, гіпоплазія придаткових порожнин носа, пальцеві вдавлення, у 72% – гіперкальцифікація основи черепа. Ознаки підвищення внутрішньочерепного тиску виявляють переважно у випадках вторинного гіпотиреозу. При вродженому гіпотиреозі череп збільшений, кістки його стовщені.
На особливу увагу при гіпотиреозі заслуговує психічний розвиток дитини. У випадку недостатнього надходження тироксину в кров знижується швидкість окисно-відновлювальних процесів та обмін речовин, що призводить до порушення живлення нервових клітин, зниження регулювальної дії кори великого мозку і судиннорухових центрів. Діти відстають у психічному розвитку від однолітків, загальмовані, пізно починають сідати, зводитися на ноги, ходити, говорити, не цікавляться іграшками, відстають у навчанні, їм важко контактувати з новими людьми.
Диагностика
Клінічні критерії: скарги пацієнта типові, виявляють брадикардію, зниження напов-нення пульсу, зміни з боку серцево-судинної системи, зниження сухожильних рефлексів, холодні кінцівки, виявлення набряків, зниження тембру голосу, сонливість, збільшення маси тіла, закрепи.
Лабораторні дослідження
При загальному аналізі крові – виявлення залізодефіцитної анемії, відносного лімфоцитозу, підвищення ШОЕ.
При біохімічному аналізі крові рівень холестерину підвищений, а лужний фосфат знижений. При гормональному обстеженні рівень тиреотропіну підвищений (що характерно для первинного гіпотиреозу), а рівень тиреоїдних гормонів – знижений. При вторинному та третинному гіпотиреозі рівні тиреотропіну й тиреоїдних гормонів знижені.
Для діагностики вторинного та третинного гіпотиреозу необхідно проводити пробу із внутрішньовенним уведенням 100 мкг тиреоліберину.
Так, при первинному гіпотиреозі спостерігається гіперергічна реакція на тироліберин, а при вторинному гіпотиреозі зменшується виділення тиреотропіну, при третинному гіпотиреозі реакція на тиреоліберин зберігається, але вона уповільнена.
Інструментальні методи дослідження
Ультразвукове дослідження щитоподібної залози. При УЗД розміри ЩЗ можуть бути нормальними, зменшеними (аплазія чи гіпоплазія) або збільшеними (вторинний гіпотиреоз при гіпертрофічній формі АІТ).
При електрокардіографічному дослідженні – брадикардія, амплітуда зубців R, P та комплексу QRS знижена, негативний зубець Т.
На ЕЕГ визначаються патологічні уповільнені хвилі та недостатня вираженість альфа-ритму.
Диференційна діагностика
Диференційна діагностика складна в період новонародженості, коли дитина ще перебуває на грудному вигодовуванні. У цей час уроджений гіпотиреоз слід диференціювати з хворобою Дауна (шляхом дослідження каріотипу), рахітом, фенілкетонурією, жовтяницею різного походження. У старшому віці диференціальну діагностику проводять із захворюваннями, що супроводжуються затримкою росту (хондродистрофія, гіпофізарний нанізм, дизгенезія статевих залоз, хвороба Пертеса, деформуючий остеохондрит). За наявності виражених набряків необхідно виключити хворобу нирок, вроджену ваду серця, ревматизм.
Гіпотиреоз слід диференціювати також із псевдогіпотиреозом, за якого порушення обміну трийодтироніну відбувається за умов збереження функції щитоподібної залози.
Лечение
Основним методом лікування гіпотиреозу є замісна терапія препаратами тиреоїдних гормонів (левотироксин).
Замісну терапію L-тироксином у разі вродженого гіпотиреозу проводять у початковій дозі 25-50 мкг/добу або 8-12 мкг/кг на добу.
При перерахунку на площу поверхні тіла доза препарату у новонароджених становить 150-200 мкг/м2, у дітей старшого віку – 100-150 мкг/м2. В подальшому дозу препарату визначають за рівнем ТТГ у крові.
Дозу левотироксину поступово зменшують з віком, але залишають однаковою на одиницю поверхні тіла – 100 мкг/м2 на добу. У разі вторинного гіпотиреозу доза тироксину становить 2-2,5 мкг/кг добу.
Рівень Т4 нормалізується через 1-2 тижні після початку лікування, а рівень ТТГ – через 3-4 тижні після початку лікування.
В комплекс лікувальних заходів при гіпотиреозі слід включати симптоматичну терапію: антианемічну (препарати заліза, вітаміни В1 і В12, фолієву кислоту) за показаннями; ноотропні препарати (ноотропіл) у вікових дозах. Тривалість курсу лікування – 1-2 міс.; вітамінотерапія (аевіт) – по 1 таблетці на день, тривалість курсу лікування –1 міс.; триметабол дітям від 1 до 3 років – по 2,5 мл 3 рази на день; дітям від 3 до 6 років – по 5-10 мл 3 рази на день; гепатопротекторні препарати (есенціале, енерлів) – по 1 капсулі 3 рази на день. Тривалість курсу лікування – 3 місяці. Рекомендується ЛФК та масаж.
Контроль за лікуванням здійснюють за оцінкою клінічної картини динаміки росту, показників диференціювання скелету (рентген-вік), загального і психічного розвитку дитини, рівня Т4 вільного і ТТГ (на першому році життя – кожні 3 міс).
Рекомендації
При задовільній компенсації гіпотиреозу діти потребують диспансерного нагляду, проведення повного ендокринологічного обстеження, корекції лікування 2-3 рази на рік. Якщо є ускладнення з боку серцево-судинної та нервової систем і скелету, огляди потрібно проводити 1 раз на 3 міс.
Юридические аспекты
Перед проведенням діагностичних та лікувальних процедур потрібно отримати згоду батьків або офіційного опікуна дитини.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



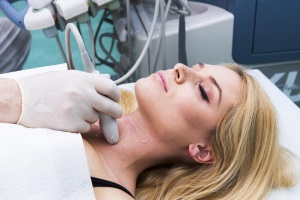 Субклінічний гіпотиреоз: стан проблеми та підходи до лікування
Субклінічний гіпотиреоз: стан проблеми та підходи до лікування
 Терапия препаратами тиреоидальных гормонов (укр)
Терапия препаратами тиреоидальных гормонов (укр)
 Йододефицит – древний спутник человечества
Йододефицит – древний спутник человечества
 Изменение нормативно-правовой документации в репродуктологии – вместо приказа № 771 появился «новорожденный» приказ № 787
Изменение нормативно-правовой документации в репродуктологии – вместо приказа № 771 появился «новорожденный» приказ № 787