- Головна
- /
- Статті
- /
- Ендокринологія. Цукровий діабет
- /
- Коматозные состояния при сахарном диабете
Коматозные состояния при сахарном диабете
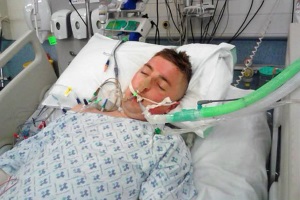
К острым осложнениям сахарного диабета (СД) относятся коматозные состояния, возникающие вследствие декомпенсации заболевания (кетоацидотическая, гиперосмолярная комы) либо в результате введения большей дозы инсулина или сахароснижающих пероральных препаратов (гипогликемическая кома). Несмотря на уменьшение случаев развития коматозных состояний в последние годы, их частота остается достаточно высокой, и терапия представляет большие сложности. Острые осложнения СД – патологические состояния, которые требуют немедленного интенсивного лечения.
 У больных СД могут развиваться такие коматозные состояния: кетоацидотическая, гиперосмолярная, гипогликемическая, молочно-кислая, а также уремическая и церебральная комы. Кетоацидотическая кома является наиболее часто выявляемым осложнением СД.
У больных СД могут развиваться такие коматозные состояния: кетоацидотическая, гиперосмолярная, гипогликемическая, молочно-кислая, а также уремическая и церебральная комы. Кетоацидотическая кома является наиболее часто выявляемым осложнением СД.
Кетоацидоз может развиваться при манифестации заболевания у лиц с впервые выявленным СД 1 типа, однако чаще данная кома возникает у пациентов, у которых диабет существует в течение определенного времени. Наиболее частыми причинами, приводящими к кетоацидозу, являются: неправильное введение инсулина, неадекватное уменьшение дозы инсулина или числа инъекций, инфекции, травмы, острые сердечно-сосудистые заболевания (инфаркт миокарда, острые нарушения мозгового, периферического кровообращения), психоэмоциональный стресс, хирургические вмешательства, прием наркотиков (кокаина).
В основе развития диабетического кетоацидоза лежат следующие патогенетические механизмы: инсулиновая недостаточность (как в результате недостаточного поступления, так и вследствие усиления потребности в инсулине на фоне имеющейся у пациентов с диабетом 1 типа абсолютной инсулиновой недостаточности), а также избыточная продукция контринсулиновых гормонов (прежде всего, глюкагона, а также кортизола, катехоламинов, гормона роста), что приводит к уменьшению утилизации глюкозы периферическими тканями, стимуляции глюконеогенеза в результате усиленного распада белка и гликогенолиза, к подавлению гликолиза в печени и, в конечном итоге, ведет к развитию выраженной гипергликемии. В свою очередь, повышенный уровень глюкозы в крови является причиной осмотического диуреза и вызывает гиповолемию, дегидратацию, потерю электролитов – натрия, калия, фосфатов и других веществ – с мочой. Уменьшение объема циркулирующей крови вызывает компенсаторное усиление продукции катехоламинов, которое еще более ухудшает действие инсулина в печени и стимулирует липолиз. Недостаточность инсулина и избыток катехоламинов способствуют мобилизации жирных кислот из жировой ткани. В этих условиях в печени вместо физиологической реэстерификации поступающих жирных кислот с формированием триглицеридов происходит усиленная продукция кетоновых тел – бета-гидроксимасляной кислоты, ацетоацетата и ацетона. Избыточная продукция кетоновых тел в печени превосходит возможности организма метаболизировать и выводить их, в результате связывания накапливающихся ионов водорода происходит снижение содержания бикарбоната и уровня рН крови, формируется метаболический ацидоз. В качестве компенсаторного ответа развивается гипервентиляция, приводящая к снижению РаСО2. Отмеченные патогенетические механизмы лежат в основе характерного клинического симптомокомплекса диабетического кетоацидоза.
Клинически кетоацидотическая кома обычно развивается постепенно, от нескольких часов до нескольких дней. Больные предъявляют жалобы на выраженные сухость во рту, жажду, полиурию, свидетельствующие о нарастании декомпенсации СД. Может регистрироваться потеря массы тела пациентов, также обусловленная декомпенсированным течением заболевания на протяжении определенного времени. По мере прогрессирования кетоацидоза появляются такие симптомы, как тошнота и рвота (указанные жалобы больного СД диктуют необходимость обязательного исследования содержания ацетона в моче). Больные могут предъявлять жалобы на сильную боль в животе, в том числе сопровождающуюся симптомами раздражения брюшины (данные проявления диабетического кетоацидоза могут приводить к ошибочной диагностике острого живота и проведению хирургического вмешательства, ухудшающего, естественно, состояние больного). Типичными клиническими симптомами развивающейся кетоацидотической комы является частое глубокое дыхание (дыхание Куссмауля), нередко с запохом ацетона в выдыхаемом воздухе. При осмотре больных наблюдается выраженная дегидратация, проявляющаяся сухостью кожи и слизистых оболочек, снижением тургора кожи. Вследствие уменьшения объема циркулирующей крови может развиваться ортостатическая гипотензия. Часто у больных отмечаются спутанность и затуманенность сознания, приблизительно в 10% случаев пациенты поступают в стационар в состоянии комы.
Наиболее типичным лабораторным проявлением кетоацидоза является гипергликемия, обычно достигающая 28-30 ммоль/л (или 500 мг/дл), хотя содержание глюкозы крови в некоторых случаях повышено незначительно. На уровень гликемии оказывает влияние и состояние функции почек, если экскреция глюкозы с мочой нарушена в результате уменьшения объема циркулирующей крови или ухудшения функции почек, гипергликемия может достигать очень высокого уровня, а также отмечаться гиперкетонемия. При определении кислотно-щелочного состояния выявляется метаболический ацидоз, характеризующийся низким уровнем рН крови (обычно в пределах 6,8-7,3 в зависимости от тяжести кетоацидоза) и снижением содержания бикарбоната в плазме крови (менее 10 мэкв/л). Уровни гипергликемии и метаболического ацидоза могут не коррелировать между собой, типичны также глюкозурия и кетонурия, позволяющие быстро установить диагноз диабетического кетоацидоза. Может изменяться содержание ряда электролитов. Содержание калия в плазме крови может быть вначале повышено (в результате перехода ионов калия из клетки во внеклеточное пространство вследствие инсулиновой недостаточности и метаболического ацидоза), несмотря на дефицит калия в организме. Позднее содержание калия снижается как вследствие усиленной потери электролитов с мочой, так и в результате терапевтической коррекции ацидоза. Осмолярность плазмы повышена (обычно превышает 300 мосм/кг). Несмотря на снижение общего содержания натрия, хлора, фосфора и магния в организме, уровни этих электролитов в сыворотке крови могут не отражать этого уменьшения. Рост содержания мочевины и креатинина в крови возникает в результате уменьшения объема циркулирующей крови. Часто отмечаются лейкоцидоз, гипертриглицеридемия и гиперлипопротеинемия, иногда выявляется гиперамилаземия, что иногда заставляет врачей задумываться о возможном диагнозе острого панкреатита, особенно в сочетании с болью в животе. Однако выявляемая амилаза продуцируется в основном в слюнных железах и не является диагностичной для панкреатита. Концентрация натрия в плазме снижена вследствие эффекта разведения, так как осмотическое действие гипергликемии ведет к увеличению количества внеклеточной жидкости. Снижение натрия в крови коррелирует с уровнем гипергликемии – на каждые 100 мг/дл (5,6 ммоль/л) уровень натрия в крови уменьшается на 1,6 ммоль/л. Если при кетоацидозе выявляется нормальное содержание натрия в крови, это может свидетельствовать о выраженном дефиците жидкости вследствие дегидратации.
В терапии диабетической кетоацидотической комы выделяют четыре направления: инсулинотерапию, восстановление потерянной жидкости, коррекцию минерального и электролитного обмена и лечение провоцирующих кому заболеваний и осложнений кетоацидоза.
Введение инсулина позволяет увеличить потребление глюкозы тканями, затормозить доставку жирных кислот и аминокислот из периферических тканей в печень. В настоящее время наиболее распространенный ранее метод массивной инсулинотерапии, заключавшийся в введении больших доз инсулина (80-300 ЕД) в течение первого часа, заменен на метод инсулинотерапии малыми дозами, позволяющий достичь более постепенного снижения показателей гликемии и уменьшить риск развития осложнений кетоацидотической комы. Следует подчеркнуть, что при терапии больного в состоянии кетоацидотической комы нужно использовать только инсулины короткого действия, в то время как инсулины среднего и длительнго действия противопоказаны до выведения пациента из состояния кетоацидоза. Наиболее эффективны человеческие инсулины, однако при лечении больных, находящихся в коматозном или прекоматозном состоянии, определяющим фактором, диктующим необходимость введения какого-либо вида инсулина, является именно длительность его действия, а не вид. Рекомендуется введение инсулина в дозе 10-20 ЕД внутривенно струйно или внутримышечно, затем внутривенно капельно – 0,1 ЕД/кг/ч или 5-10 ЕД /ч. Обычно гликемия снижается со скоростью 4,2-5,6 ммоль/л/ч. Если в течение 2-4 часов уровень гипергликемии не уменьшается, доза вводимого инсулина увеличивается в 2-10 раз. При снижении гликемии до 14 ммоль/л скорость введения инсулина уменьшается до 1-4 Ед/ч. Определяющим в выборе скорости и дозы введения инсулина является постоянный контроль содержания глюкозы крови. Желательно проведение анализа крови каждые 30-60 минут с помощью экспресс-анализаторов глюкозы (следует помнить, что многие используемые сейчас с целью самоконтроля экспресс-анализаторы глюкозы могут показывать неправильные цифры гликемии при высоком уровне сахара в крови). Состояние кетоацидоза характеризуется выраженной инсулинорезистентностью периферических тканей, в связи с этим доза инсулина, необходимая для выведения больного из коматозного состояния, может оказаться весьма высокой, значительно превышая обычные дозы инсулина, необходимые больному до или после кетоацидоза. Только после полной коррекции гипергликемии и купирования кетоацидоза можно назначать больному инсулины средней продолжительности действия подкожно в качестве так называемой базисной терапии. Непосредственно после выведения больного из состояния кетоацидоза чувствительность тканей к инсулину резко возрастает, поэтому нужны контроль и коррекция дозы инсулина с целью предотвращения гипогликемических реакций.
Учитывая характерную дегидратацию в результате осмотического диуреза, обусловленного гипергликемией, необходимым элементом терапии больных с кетоацидотической комой является восстановление объема жидкости. Обычно у пациентов отмечается дефицит жидкости, в 3-5 л, который должен быть полностью замещен. С этой целью рекомендуется введение 2-3 л 0,9% физиологического раствора в течение первых 1-3 часов или 5-10 мл/кг/ч. Затем (обычно при повышении концентрации натрия в плазме выше 150 ммоль/л) назначается внутривенное введение 0,45% раствора Na с меньшей скоростью – 150-300 мл/ч с целью коррекции гиперхлоремии. При снижении уровня глюкозы крови до 15-16 ммоль/л (250 мг/дл) необходимо вводить инфузионно 5% раствор глюкозы для предотвращения гипогликемии и обеспечения доставки глюкозы тканям наряду с 0,45% раствором хлорида натрия со скоростью 100-200 мл/ч. При этом следует помнить, что достижение стойкой нормогликемии не является непосредственной целью терапии больных в состоянии кетоацидотической комы на первом этапе. В случае, если при снижении уровня гликемии у больного сохраняется дегидратация, введение глюкозы проводят параллельно с физиологическим раствором. Замещение объема жидкости, наряду со стабилизирующим гемодинамическим действием, способствует снижению гликемии (даже без введения инсулина) путем уменьшения содержания катехоламинов и кортизола в плазме крови (выброс которых происходит в ответ на уменьшение объема циркулирующей крови).
Необходима коррекция содержания минералов и электролитов, потерянных вследствие осмотического диуреза. Важна также коррекция содержания в плазме крови калия, запасы которого в организме невелики. Если исходно наблюдается гиперкалиемия, введение растворов, содержащих калий, следует отложить, пока уровень данного электролита в плазме станет нормальным или пониженным в результате проводимой терапии. Рекомендуется введение 10 мэкв/ч калия при снижении его уровня менее 5,5 ммоль/л, а при уменьшении ниже 3,5 ммоль/л количество вводимого калия следует увеличить до 40-80 мэкв/ч. Также возможно назначение фосфата калия в зависимости от содержания в плазме крови кальция и фосфора – слишком интенсивное введение фосфата калия может вызвать гипокальциемию. Следует корригировать содержание фосфатов в плазме крови, вводя 10-20 ммоль/ч фосфата калия, максимально до 40-60 ммоль. Введение бикарбоната натрия с целью коррекции кетоацидоза (столь широко практикуемое в ряде отделений интенсивной терапии) проводят только в случае, если рН крови снижается ниже 7,0. Поскольку диабетический кетоацидоз корригируется введением инсулина и жидкости, избыточное назначение бикарбоната может привести к развитию алкалоза. Некоторые специалисты рекомендуют начинать введение бикарбоната, только если рН падает ниже 6,9.
Важные направления в терапии кетоацидотической комы – выявление и лечение сопутствующих заболеваний, которые могли послужить причиной развития кетоацидоза, а также ухудшить его течение. Так, необходимо тщательно обследовать больного с целью диагностики и лечения инфекционных заболеваний, особенно инфекций мочевыводящих путей. В случае подозрения на наличие у больных инфекции целесообразно назначить антибиотики широкого спектра действия. Учитывая характерные нарушения сознания у пациентов, определенную сложность может представлять диагностика менингита, инсульта, инфаркта миокарда. Часто необходимо проведение аспирации желудочного содержимого, особенно в случаях, если больной без сознания и у него отмечаются рвота или дилатация желудка. При падении артериального давления, несмотря на проводимое введение жидкости, возможно переливание цельной крови или плазмозамещающих растворов.
Гипогликемическая кома развивается при резком снижении уровня сахара в крови – обычно до 2 ммоль/л и менее, также вследствие ряда причин у лиц, не болеющих СД. У больных диабетом гипогликемическая кома может быть вызвана такими факторами, как большая доза инсулина, задержка приема пищи, усиленная физическая активность. Сахароснижающие таблетированные препараты – производные сульфонилмочевины – также могут вызвать гипогликемию, однако значительно реже, чем инсулин. Выраженное гипогликемическое действие может оказывать и избыточный прием алкоголя. Больные СД предрасположены к гипогликемии в результате недостаточной продукции контринсулиновых гормонов (глюкагон, адреналин). Нужно подчеркнуть, что у больных диабетом может отмечаться так называемый синдром атипичных гипогликемий, в результате которого у пациентов развивается гипогликемическая кома без предшествующих симптомов активации симпатоадреналовой системы (в основе данного синдрома предположительно лежат длительное течение заболевания, вегетативная нейропатия, частые гипогликемии в анамнезе).
Клинические симптомы гипогликемии развиваются в течение короткого промежутка времени и обусловлены активацией симпатоадреналовой системы (потливость, тремор рук, сердцебиение), при дальнейшем снижении уровня гликемии – нейрогликопенией, проявляющейся головной болью, затруднением речи, нарушениями сознания с появлением очаговой неврологической симптоматики и судорог вплоть до развития комы.
Диагноз гипогликемии обычно не представляет трудности, если больной в сознании и имеются характерные симптомы и данные анамнеза. Вместе с тем при поступлении больного с СД, находящегося в коматозном состоянии, требуется провести тщательную дифференциальную диагностику с целью выяснения причины комы. Низкий уровень глюкозы в крови подтверждает диагноз гипогликемической комы.
При подтверждении диагноза гипогликемической комы лечение заключается во введении 50 мл 50% раствора глюкозы внутривенно (при невозможности перорального питания пациента) в течение 3-5 минут с последующей капельной инфузией 5 или 10% раствора глюкозы. У некоторых больных восстановление сознания происходит непосредственно после введения глюкозы, у других занимает определенное время. Внутривенное введение глюкозы должно продолжаться в течение всего ожидаемого периода действия инсулина или перорального сахароснижающего препарата, вызвавшего данную кому (например, если кома вызвана приемом хлорпропамида, введение глюкозы следует проводить в течение нескольких дней). Дополнительно рекомендуется введение 1 мг глюкагона внутримышечно. После купирования комы следует провести коррекцию сахароснижающей терапии, диеты и режима больного.
Гиперосмолярная кома выявляется значительно реже, чем кетоацидотическая, однако характеризуется более высокой смертностью, достигающей 60%. Гиперосмолярная кома обычно развивается у пожилых больных, в основном 2 типа диабета, причем в 60% случаев диагноз СД не был установлен до наступления комы. В возникновении этой комы играют роль ряд провоцирующих факторов – инфекции, другие сопутствующие заболевания, увеличенное потребление глюкозы с пищей, отказ от введения инсулина, прием медикаментозных средств (кортикостероиды, тиазидовые диуретики, фенитоин) и другие причины, способствующие нарастанию гипергликемии в течение нескольких дней или недель. Развивающийся вследствие этого осмотический диурез, некомпенсируемый адекватным поступлением жидкости в организм, приводит к выраженной дегидратации и прогрессирующему нарушению сознания. Характерным признаком гиперосмотической комы является отсутствие кетоацидоза, так как сохраняющаяся у больных СД 2 типа секреция инсулина достаточна, чтобы предотвратить кетогенез в печени, но недостаточна для поддержания нормогликемии. Клинически больные предъявляют жалобы на нарастающие в течение нескольких дней или недель сильную жажду, полиурию. При обследовании пациентов с гиперосмолярной комой выявляют выраженную дегидратацию (большую, чем при кетоацидотической коме, в результате более длительного периода осмотического диуреза до развития комы), артериальную гипотензию, очень высокий уровень гликемии, достигающий 55 ммоль/л (1000 мг/л). Характерна высокая осмолярность плазмы крови (более 360 мосм/кг). Для расчета осмолярности применяется следующая формула: осмолярность (мосм/кг) = 2 (Na++ K+) ммоль/л + гликемия (ммоль/л) + мочевина (ммоль/л).
Дегидратация и гиперосмолярность приводят к нарушению сознания, судорогам и очаговой неврологической симптоматике. В ряде случаев гиповолемия может приводить к появлению лактатоцидоза, ухудшающего прогноз комы.
Основными принципами терапии гиперосмолярной комы являются замещение потерянной жидкости и коррекция гипергликемии путем введения инсулина. Учитывая высокую осмолярность плазмы, характерную для больных с гиперосмолярной комой, целесообразно назначение гипотонического 0,45% физиологического раствора для восстановления жидкостного баланса в организме, если содержание натрия в крови более 150 ммоль/л. Обычно вводят 1-3 л раствора в течение 2-3 часов. После стабилизации показателей гемодинамики продолжают введение жидкости для возмещения ее дефицита, который обычно достигает 9-10 л, в течение 1-2 дней со скоростью 200-300 мл гипотонического раствора в час. Введение жидкости, особенно у пожилых пациентов с сопутствующей сердечно-сосудистой патологией, должно осуществляться под контролем показателей центрального венозного давления для профилактики гиперволемии и последующей сердечной недостаточности. Следует проводить также контроль и коррекцию уровня калия, фосфора и магния в крови пациентов. Также необходимымо введение инсулина, хотя и в меньших дозах, чем при кетоацидотической коме обычно 5-10 ЕД инсулина короткой продолжительности действия внутривенно струйно, затем – 3-7 Ед/ч внутривенно капельно. При снижении гликемии до 250 мг/мл (13,9 ммоль/л) добавляется введение 5% раствора глюкозы, а скорость введения инсулина снижается до 1-2 Ед/ч.
Лактатацидемическая кома сопряжена с наибольшей частотой летальных исходов – смертность может достигать 80%. Состояние лактатацидоза констатируется при повышении уровня молочной кислоты в плазме крови свыше 5 ммоль/л и снижении рН артериальной крови ниже 7,2. Лактатацидемическая кома не является специфическим острым осложнением сахарного диабета и может развиваться при ряде состояний, при которых отмечаются явления аноксии и шока (инфаркт миокарда, заболевания печени, почек, лейкемия, ферментативные расстройства и другие). СД сам по себе редко приводит к лактатацидозу, хотя раньше отмечались случаи лактатацидоза у больных, получавших терапию бигуанидом фенформином и, в меньшей степени, буформином, однако при применении другого препарата из группы бигуанидов – метформина – данное осложнение выявляется крайне редко.
Симптомы лактатацидоза в основном обусловлены сдвигами кислотно-щелочного состояния. В клинической картине на первый план выступает быстро прогрессирующая сердечно-сосудистая недостаточность, ведущая к развитию коллапса, артериальной гипотонии, гипоксии мозга и нарушению сознания. Характерна гипервентиляция, однако дегидратация выражена нерезко. Уровень глюкозы крови может значительно варьировать, и у некоторых пациентов отмечается гипогликемия. Поскольку симптомы лактатацидоза неспецифичны, диагноз лактатацидемической комы должен быть заподозрен у больного СД с гипотензией или в состоянии шока в случае, если выраженность ацидоза не соответствует степени кетоза. Хотя у всех больных с лактатацидозом отмечается некоторое повышение уровня кетоновых тел в крови, при этом он обычно не превышает 1/3 общего содержания органических кислот. Таким образом, диагноз лактатацидемической комы во многом – диагноз исключения. Окончательный диагноз устанавливается на основании определения содержания молочной кислоты в крови.
В настоящее время не существует эффективных методов терапии лактатацидемической комы. Основная в лечении – коррекция нарушений циркуляции и устранение артериальной гипотензии, другой важный момент – коррекция ацидоза. С этой целью обычно необходимо вводить большее количество бикарбоната натрия, часто превышающее 1000 ммоль, что, в свою очередь, может повышать содержание натрия в организме и диктовать необходимость проведения гемодиализа или перитонеального диализа для коррекции гипернатриемии. Эффективность применения других терапевтических средств при лактатацидозе, таких как дихлорацетата (активатора пируват дегидрогеназы), буферных растворов или метиленового синего, остается недоказанной.
Литература
- Ефимов А.С., Комиссаренко И.В., Скробонская Н.А. Неотложная эндокринология. – М.: Медицина, 1982. – 208 с. 14.
- Балаболкин М.И., Лукьянчиков В.С. Клиника и терапия критических состояний в эндокринологии. – Киев: Здоров’я, 1982. – 152 с.
- Балаболкин М.И. Сахарный диабет. – М.: Медицина, 1994. – 384 с.
- Carr D. Devising a protocol for managing diabetic ketoacidosis in adults // Practical Diabetes. – 1995. – V. 12, N 4. – P. 164-169.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Осложнения сахарного диабета. Воздействуем на механизм
Осложнения сахарного диабета. Воздействуем на механизм
 Тиоктовая кислота в профилактике осложнений сахарного диабета
Тиоктовая кислота в профилактике осложнений сахарного диабета
 Особенности приема витаминов и минералов при сахарном диабете
Особенности приема витаминов и минералов при сахарном диабете
 Применение нейропротекторов при неврологических осложнениях сахарного диабета
Применение нейропротекторов при неврологических осложнениях сахарного диабета