- Головна
- /
- Статті
- /
- Урологія і нефрологія
- /
- Хроническая болезнь почек и хроническая почечная недостаточность у детей
Хроническая болезнь почек и хроническая почечная недостаточность у детей
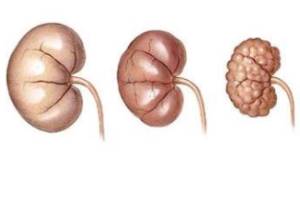
В последние годы современная нефрология столкнулась, по крайней мере, с тремя очень важными проблемами. Во-первых, наблюдается фактическое увеличение количества больных с хронической почечной патологией. Во-вторых, результаты этиологического и патогенетического лечения большинства хронических болезней почек остаются несовершенными.
тематический номер: ПЕДИАТРИЯ, АКУШЕРСТВО, ГИНЕКОЛОГИЯ
В-третьих, оба вышеперечисленных фактора привели к увеличению количества пациентов, которым требуется заместительная почечная терапия (ЗПТ). Однако следует признать, что росту числа пациентов на ЗПТ способствовал и существовавший долгое время подход ко вторичной профилактике терминальной почечной недостаточности у больных с хронической почечной патологией. Считалось, что поскольку рано или поздно применение ЗПТ все равно потребуется, то с достижением определенной степени снижения функции почек прибегать к каким-либо специальным методам замедления прогрессирования патологического процесса в почечной ткани нет необходимости. Кроме того, на протяжении последних десятилетий непрерывно улучшалось качество технологий ЗПТ, что вызвало резкое увеличение продолжительности жизни больных, получающих такие методы лечения. Все это привело к тому, что требовалось все больше и больше диализных мест или органов для трансплантации, катастрофически росли расходы. К примеру, в США и Японии количество пациентов, получающих ЗПТ, в настоящее время составляет более 1400 человек на 1 млн населения. Организационные и финансовые проблемы, связанные с ЗПТ, начали превышать возможности даже высокоразвитых стран.
 Выходу из сложившейся ситуации способствовали два фактора. В настоящее время достигнуты значительные успехи в раскрытии патогенетических механизмов прогрессирования хронических заболеваний почек. При этом особое внимание уделяется так называемым неиммунным факторам (функционально-адаптивным, метаболическим и др.). Такие механизмы в той или иной степени действуют при хронических поражениях почек любой этиологии, значимость их возрастает по мере уменьшения количества действующих нефронов, и именно эти факторы во многом определяют скорость прогрессирования и исход заболевания.
Выходу из сложившейся ситуации способствовали два фактора. В настоящее время достигнуты значительные успехи в раскрытии патогенетических механизмов прогрессирования хронических заболеваний почек. При этом особое внимание уделяется так называемым неиммунным факторам (функционально-адаптивным, метаболическим и др.). Такие механизмы в той или иной степени действуют при хронических поражениях почек любой этиологии, значимость их возрастает по мере уменьшения количества действующих нефронов, и именно эти факторы во многом определяют скорость прогрессирования и исход заболевания.
Механизмы прогрессирования хронических заболеваний почек
Функционально-адаптивные: гиперперфузия и гиперфильтрация в клубочках, внутриклубочковая гипертензия, гипоперфузия почек, гипоксия интерстиция, нарушение почечного транспорта белка (протеинурия).
Структурно-клеточные адаптивные: увеличение диаметра капилляров клубочка, гипертрофия структур почек, дисбаланс между синтезом и деградацией матрикса соединительной ткани почек, гломерулосклероз, тубулоинтерстициальный склероз.
Изменения экспрессии медиаторов клеточного и структурного повреждения: цитокинов, факторов роста, пептидов.
Метаболические и эндокринные: высокое потребление белка, дислипопротеидемия, нарушения минерального обмена, гиперпаратиреоидизм, гиперурикемия, анемия.
Врожденные и генетические факторы: врожденное уменьшение количества нефронов, полиморфизм генов, контролирующих экспрессию нефротропных биологически активных веществ.
Уточнение механизмов патогенеза и факторов риска дало возможность разработать вполне обоснованные схемы консервативной терапии и подходы к профилактике, позволяющие в какой-то мере предупреждать и достаточно эффективно контролировать течение болезни, значительно отдалять начало ЗПТ, уменьшать количество осложнений. Помимо создания целого комплекса мер, превентивный подход потребовал от нефрологов разработки и новых ориентиров, которые позволяли бы правильно выбирать необходимые вмешательства в соответствии с этапами развития заболевания. Все это требовало создания элементов «энциклопедического словаря медицинских терминов», в котором давались бы принятые всем нефрологическим сообществом единые трактовки основополагающих понятий клинической нефрологии. Актуальным оставался вопрос о выделении критериев, позволяющих по единым принципам оценивать тяжесть заболевания почек, его прогноз, необходимость и целесообразность использования тех или иных терапевтических воздействий на определенных этапах развития болезни.
Решение этих проблем предложил Национальный почечный фонд США (NKF, 2003). Для этой цели была создана группа экспертов, включая специалистов в области нефрологии, детской нефрологии, эпидемиологии, клинической лабораторной диагностики, диетологии, социальной деятельности, геронтологии, а также семейной медицины. В результате анализа многих публикаций по вопросам диагностики и лечения, оценки значимости ряда показателей в детерминации скорости прогрессирования заболеваний почек, терминологических понятий и согласований с представителями администрации было предложено понятие хронической болезни почек (ХБП, CKD – chronic kidney disease). Вводя концепцию ХБП, эксперты рабочей группы NKF преследовали ряд целей.
Основные цели рабочей группы по созданию концепции ХБП:
- определение понятия ХБП и ее стадий независимо от причины (этиологии) почечной недостаточности (заболевания);
- выбор лабораторных показателей (методов исследования), адекватно характеризующих течение ХБП;
- определение (изучение) связи между степенью нарушения функции почек и осложнениями ХБП;
- стратификация факторов риска прогрессирования ХБП и возникновения сердечно-сосудистых заболеваний.
В 2005 г. самая авторитетная организация – KDIGO (Kidney Diseases: Improving Global Outcomes) – подтвердила инициативу K/DOQI 2003 г. широкого использования термина ХБП [3]. В МКБ-0 ХБП не классифицируется. Вместе с тем в международной классификации ICD-9-CM, начиная с 1 октября 2005 г., всем пяти стадиям ХБП уже были присвоены свои коды.
С 2003 г. в детской нефрологии также используется понятие ХБП. Этот термин заимствован из терапевтической нефрологии и впервые был представлен в журнале Pediatrics R.J. Hogg с соавт. в 2003 г. [1, 9]. Критерии определения ХБП у взрослых и детей идентичны (www.nephrology.kiev.ua).
Кроме определения уровня СКФ, существуют также методы оценки индивидуальной скорости прогрессирования ХБП, расчет которой производится по методу Mitch и соавт. по показателям величины, обратной уровню креатинина плазмы (1/Scr).
Каким образом соотносятся стадии ХБП и ХПН у детей? На сегодня в Украине мы используем классификацию, очень схожую с таковой у взрослых, утвержденную приказом МЗ Украины № 365 от 20 июля 2005 г. и ІІ съездом нефрологов Украины (сентябрь, 2005) (http://72.14.221.104/u/kidney); Anemia and CKD, 2006. На стадии завершения находятся рекомендации Diabetes and CKD, Vascular Access, Updates: Peritoneal Dialysis Adequacy, Hemodyalisis Adequacy. Рекомендации Европейской ассоциации нефрологов, диализатологов и трансплантологов, которые пользуются термином ХБП, представлены по проблемам лечения анемии и перитонеального диализа. Существуют адаптации мировых руководств к потребностям отдельных стран: рекомендации по определению ХБП (Канада, 2004; Великобритания, 2006). Некоторые рекомендации переведены на украинский и русский языки [11].
В соответствии с рекомендациями ERA-EDTA 2004 [2], анемией у пациентов с ХБП считается снижение гемоглобина более чем на 2 сигмы (95%) от нормальных значений в популяции, а именно:
- менее 115 г/л у взрослых пациентов женского пола (менее 120 г/л согласно K/DOQI, 2006);
- менее 135 г/л у взрослых пациентов мужского пола (для всех мужчин независимо от возраста согласно K/DOQI, 2006);
- менее 120 г/л у мужчин старше 70 лет (уровень доказательности В).
Анемией у детей до 6-летнего возраста считается уровень гемоглобина менее 110 г/л, от 6 лет до пубертатного возраста – ниже 120 г/л согласно рекомендациям ВОЗ и менее 110 г/л – в соответствии с EBPG, 1999.
До назначения специфического лечения эритропоэтинстимулирующим агентом (ЭСА) у пациентов с анемией на фоне ХБП следует провести клинические и диагностические исследования, которые позволят обосновать тактику лечения и определить существующие дефициты (например, железа).
Для диагностики анемии используют следующие лабораторные параметры:
- концентрация гемоглобина – для установления степени анемии;
- MCV (средний объем эритроцита) и MCH (среднее содержание гемоглобина в эритроците) – для определения типа анемии;
- абсолютное число ретикулоцитов – для оценки активности эритропоэза;
- содержание ферритина плазмы/сыворотки – для определения депо железа;
- процент гипохромных эритроцитов или сатурация трансферрина или содержание ретикулоцитов – для оценки функциональной доступности железа;
- С-реактивный белок плазмы/сыворотки – для определения воспаления (уровень доказательности В).
У пациентов, получающих диализ, необходимо учитывать частоту процедур и диализную дозу.
В лечении анемии у пациентов с ХБП целевым является уровень гемоглобина более 110 г/л (гематокрит более 33%), который должен быть достигнут не позднее 4 месяцев после начала лечения независимо от возраста, пола и расы пациента. Дальнейший прирост гемоглобина определяется индивидуально, учитывая пол, возраст, расу, активность пациента и сопутствующую патологию.
Пациенты с ХБП должны иметь сбалансированный железный статус или достаточно железа, чтобы поддерживать концентрацию гемоглобина свыше 110 г/л и гематокрит 33%. Для достижения целевого гемоглобина следует назначать терапию препаратами железа для обеспечения:
- сывороточного ферритина более 100 мкг/л;
- количества гипохромных эритроцитов менее 10% (или сатурации трансферрина более 20%, или концентрации гемоглобина ретикулоцитов более 29 пг в клетке).
На практике для достижения приведенных минимальных уровней целесообразно ориентироваться на уровень ферритина 200-500 мкг/л, содержание гипохромных эритроцитов менее 2,5% (или сатурации трансферрина 30-40%, или концентрации гемоглобина ретикулоцитов 35 пг/клетку).
Лечение ХБП проводится с использованием препаратов железа (для в/в введения применяют Феролек-Здоровье, Венофер) и эритропоэтины.
Препараты эритропоэтина необходимо использовать постоянно в качестве заместительной терапии. Показателем эффективности терапии эритропоэтином у детей с ХПН является прирост гемоглобина более 12-20 г/л в месяц (гематокрита более 2%). Перед назначением эритропоэтина необходимо провести коррекцию дефицита железа, белка и витаминов.
Доза железа должна составлять не менее 200 мг элементарного железа в сутки для подростков и 2-3 мг/кг – для детей. Коррекция дефицита белка проводится путем назначения незаменимых аминокислот (кетостерил) и специальных пищевых смесей. С целью пополнения содержания витамина В12 применяют цианокобаламин и оксикобаламин. Цианокобаламин назначается в дозе 400-500 мкг один раз в сутки на протяжении 4-6 недель. Оксикобаламин применяется в дозе 1 мг в сутки через день. В поддерживающем режиме цианокобаламин вводят один раз в неделю в течение 2 месяцев, а потом 2 раза в месяц по 400-500 мкг. Оксикобаламин можно вводить реже: на протяжении первых 3 месяцев – один раз в неделю, потом один раз в месяц по 500 мкг. С целью пополнения дефицита фолиевой кислоты ее назначают из расчета 5-15 мг/сут в течение 2-3 недель.
Нами используется следующая схема лечения анемии у детей с ХПН.
У детей на додиализном и диализном этапах лечения при уровне гемоглобина <90 г/л целесообразно назначение ЭСА в дозе 50 МЕ/кг/нед подкожно, при уровне гемоглобина <90 г/л – 100 МЕ/кг/нед у подростков и детей с массой тела свыше 20 кг, у детей с массой тела до 20 кг – 200 МЕ/кг/нед. Кратность введения ЭСА составляет от 1 до 3 раз в неделю. При достижении целевого уровня гемоглобина переходят на поддерживающее лечение: дозу снижают на 50%, которую можно вводить 1 раз в неделю или 1 раз в 2 недели.
При недостаточном повышении уровня гемоглобина и гематокрита (прирост гемоглобина <12-20 г/л или гематокрита <2% в месяц) дозу ЭСА необходимо увеличить в 1,5-2 раза по сравнению с предыдущей до достижения эффекта.
Контроль уровня гемоглобина и гематокрита на фоне лечения ЭСА следует проводить через 1-2 недели от начала лечения или после изменения назначенной дозы и до достижения целевых значений гемоглобина и гематокрита. После ликвидации анемии мониторинг гематокрита и гемоглобина проводится с частотой 1 раз в 4 недели.
L-карнитин, аскорбат и андрогены не рекомендуются в лечении анемии согласно K/DOQI, 2006.
Нарушение фосфорно-кальциевого обмена занимает одно из ведущих мест в патогенезе и течении ХПН, особенно у детей. Значимые признаки развития гиперпаратиреоза появляются при уровне клубочковой фильтрации менее 60 мл/мин, поэтому именно с этого уровня рекомендуется наблюдение за такими пациентами. Содержание СаxР>4,44 (2,4x1,8=4,44) ммоль2/л2 и паратгормона (ПТГ) более 70 пг/мл свидетельствует о наличии гиперпаратиреоза (NKF-K/DOQI, 2003) и требует коррекции.
Выделяют три главных типа ренальной остеодистрофии, сопровождающей ХПН:
- адинамическая болезнь (медленная резорбция с отсутствием ремодуляции);
- остеомаляция (нормальная или сниженная резорбция);
- фиброзный остеит – osteitis fibrosa (быстрая резорбция костей).
В зависимости от степени ХБП рекомендуется следующая периодичность исследования ПТГ, фосфора и кальция (www.kidney.org/professionals/kdoqi/guidelines_bp/index.htm (National Kidney Foundation)
17. www.nephrology.kiev.ua (перший український нефрологічний сайт)
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Ингибиторы АПФ при хронической болезни почек: выбор препарата в зависимости от риска кардиоваскулярных или ренальных событий
Ингибиторы АПФ при хронической болезни почек: выбор препарата в зависимости от риска кардиоваскулярных или ренальных событий
 Раннее течение хронической почечной недостаточности у детей
Раннее течение хронической почечной недостаточности у детей
 Антигипертензивная терапия хронических заболеваний почек
Антигипертензивная терапия хронических заболеваний почек
 Нефропротекция. Специалисты рекомендуют
Нефропротекция. Специалисты рекомендуют