- Головна
- /
- Статті
- /
- Інфекційні захворювання
- /
- Роль и место тканевых паразитозов в патологии человека
Роль и место тканевых паразитозов в патологии человека
Развернутая клиническая картина характеризуется расширением вен на передней брюшной стенке, варикозным расширением вен пищевода и желудка, геморроидальных вен, гепато-, спленомегалией, геморрагическими проявлениями (кровотечения из вен пищевода и кардиальной части желудка, слизистой оболочки носа, десен, маточные и геморроидальные кровотечения).
Окончание. Начало в № 7/1, 8.
Наиболее характерным из местных симптомов при альвеококкозе является увеличение и асимметрия живота – определение бугристых железоподобной плотности опухолевидных образований, связанных с паренхимой печени, которые имеют важное диагностическое значение.
При появлении признаков мочевого синдрома у этих больных следует думать о поражении почек и сдавливании их извне или о росте метастазирования, приводящего к нарушению почечного кровотока и пассажа мочи, развитию восходящей инфекции мочевыводящих путей. Присоединение иммунопатологических процессов ведет к формированию хронического гломерулонефрита, системного амилоидоза с хронической почечной недостаточностью. У некоторых больных возможны геморрагические проявления по типу болезни Шенлейн-Геноха [1, 2, 5].
Существенной особенностью альвеококкоза является корреляция между частотой анемии и степенью ее выраженности, с одной стороны, и стадией выраженности патологического процесса – с другой. Это позволяет подчеркнуть зависимость анемии от длительности и степени воздействия токсических продуктов на организм. У всех больных повышено СОЭ. Эозинофилия при альвеококкозе является выражением степени аллергических реакций. Лимфопения чаще наблюдается при осложненных формах заболевания. Возрастные частоты и величины показателей анемии, СОЭ, общего белка и белковых фракций прямо пропорциональны стадии заболевания. Протеинограмма, функциональные пробы печени, осадочные реакции, острофазовые показатели на ранних стадиях альвеококкоза не изменяются, а при поздних становятся резко положительными в зависимости от заинтересованности того или другого органа.
Наибольшее значение в постановке диагноза играют серологические методы диагностики – ИФА, РЛА, причем их титр зависит от характера и длительности процесса.
Для уточнения локализации паразитарных узлов и их величины применяют УЗИ, компьютерную томографию, лапароскопию, сканирование с помощью радионуклидов. На сканограммах удается обнаружить дефект накопления радионуклида в печеночной ткани в местах расположения узлов альвеококка. У больных альвеококкозом печени при лапароскопии на темном фоне печени наблюдаются белесоватые или перламутрово-желтые пятна.
Большое значение в диагностике заболевания имеет пункционная биопсия, но ее целесообразно проводить только после исключения эхинококкоза. Биопсию лучше проводить во время лапароскопического исследования.
Альвеококкоз печени необходимо дифференцировать с гидатидным эхинококкозом, циррозом и новообразованиями печени. Трудности встречаются при дифференцировании альвеококкоза и гидатидного эхинококкоза, так как все симптомы, лабораторные и серологические тесты, характерные для последнего, могут наблюдаться при обоих заболеваниях. Более того, симптом железоподобной плотности печени может наблюдаться и при обызвествленном эхинококкозе. В таком случае помогает рентгенографическое исследование, при котором выявление сферически компактных участков обызвествления свидетельствует о гидатидном эхинококкозе, отличаясь от известковых брызг при альвеококкозе. Установлению диагноза помогает знание особенностей эндемического очага.
Отличить альвеококкоз от цирроза печени, несмотря на имеющиеся схожие нарушения со стороны функции печени, помогают отсутствие эозинофилии и отрицательные серологические тесты.
При дифференциации со злокачественными новообразованиями печени учитывается анамнез, а также то, что при альвеококкозе печень значительно плотнее, отсутствует кахексия, а специфические реакции положительные.
Цистицеркоз – антропонозный биогельминтоз, обусловленный паразитированием в тканях человека цистицерка Cysticercus cellulosae (финны) – личиночной стадии свиного цепня Taenia solium.
Возбудителем этого заболевания является цистицерк (личиночная стадия) ленточного гельминта Taenia solium, который относится к типу Plathelminthes (плоских червей) класса Cestoidea. Место обитания зрелого паразита – тонкий кишечник человека. Он имеет лентовидное тело (стробила) длиной 1,5-2 м, состоящее из 800-1000 члеников (проглоттид), головку (сколекс) около 1-2 мм в диаметре, 4 крестообразно расположенные присоски и хоботок, на котором находится двойная «корона» из 22-32 крючьев.
Наиболее часто освободившиеся из яйцевых оболочек онкосферы гематогенно распространяются в мышцы языка, туловища и конечностей, подкожную клетчатку, головной мозг, переднюю камеру и стекловидное тело глаза, реже в сердце, легкие, печень, брюшную полость, кости. Через 60-70 суток они превращаются в пузырьковидные личинки с ввернутым сколексом – цистицерки, вокруг которых образуется реактивная фиброзная капсула, развиваются воспалительные и дегенеративные изменения. В мозговой ткани, окружающей капсулу, развивается эндартериит и инфильтрация периваскулярных тканей преимущественно плазматическими клетками.
Цистицеркоз относится к хроническим инвазиям длительностью 10-15 лет и более. В доклинический период, несмотря на поражения мышц и подкожной клетчатки, жалобы, как правило, отсутствуют. Могут пальпироваться плотные узелки в тканях. При цистицеркозе головного мозга больных беспокоят приступообразные головные боли, тошнота, рвота, эпилептиформные приступы. Иногда нарушается психика в виде делириозных, галлюцинаторных и аментивных состояний, которые могут внезапно исчезать и вновь появляться. Цистицеркоз желудочков мозга сопровождается проявлениями внутричерепной гипертензии, цистицеркоз глаз вызывает нарушения зрения, нередко – слепоту, при поражении орбиты развивается экзофтальм. Локализация цистицерка в сердце может способствовать развитию нарушений ритма и проводимости [1, 5, 7].
Гемограмма при цистицеркозе не всегда показательна, в ней могут отмечаться невысокие значения эозинофилии, характерные для цистицеркоза глаз. Результаты серологических исследований (ИФА крови и ликвора) могут быть ложноположительными при наличии других инвазий. При выявлении титров антител ниже диагностических необходимо повторить их в динамике через 1-2 мес.
Паразитологическое исследование часто бывает затруднительным из-за невозможности получения биопсийного материала. В диагностике цистицеркоза помогает выявление у пациентов в фекалиях яиц тениид и зрелых члеников свиного цепня.
При цистицеркозе головного мозга проводят исследование ликвора, который характеризуется лимфоцитарным плеоцитозом, преобладанием эозинофилов, увеличенным содержанием белка. Для подтверждения диагноза цистицеркоза проводят УЗИ, КТ и МРТ внутренних органов [4, 5].
Дифференциальный диагноз цистицеркоза проводится с опухолями, эхинококкозом, нейроинфекциями, а при поражении глаз – токсокарозом.
Основные принципы лечения тканевых гельминтозов
Несомненным достижением последних лет является открытие и внедрение в практику новых противогельминтных препаратов. Лечение больных тканевыми гельминтозами независимо от формы и тяжести заболевания проводят в стационаре. Оно должно быть комплексным, т. е. специфическая терапия должна сочетаться с лечением, направленным на восстановление и нормализацию органов, вовлеченных в патологический процесс. Постельный режим назначают в остром периоде заболевания при тяжелых формах трихинеллеза, токсокароза, цистицеркоза, осложненных формах эхинококкоза (разрыв или нагноение эхинококковой кисты). Показана полноценная диета, обогащенная витаминами.
Этиотропная терапия показана при всех формах тканевых гельминтозов. В Украине применяются такие эффективные противопаразитарные средства, как албендазол, мебендазол и празиквантел.
Универсальным эффективным антигельминтным средством является албендазол, обладающий широким спектром активности, что особенно важно при микст-инвазиях. Он оказывает терапевтическое действие при поражениях круглыми, плоскими (в том числе свиным цепнем) червями и их личинками. Албендазол всасывается в желудочно-кишечном тракте на 30%, прием жирной пищи повышает всасывание препарата в 5 раз, что необходимо учитывать при его назначении [1, 3, 6].
При токсокарозе и трихинеллезе албендазол назначают пациентам с массой тела более 60 кг по 400 мг 2 раза в день, менее 60 кг – по 200 мг 2 раза в день, курс лечения от 7 до 14 дней в зависимости от давности и тяжести заболевания. При эхинококкозе и цистицеркозе албендазол назначают пациентам с массой тела более 60 кг по 400 мг 2 раза в день, менее 60 кг – из расчета 15 мг/кг/сут в два приема, курс терапии составляет 28 дней. Для лечения эхинококкоза рекомендовано проводить 3 курса терапии с интервалом 2 нед. В случаях неосложненного эхинококкоза печени возможно медикаментозное излечение. При субарахноидальном расположении цистицерка или его локализации в бороздах мозга албендазол применяется в течение не менее 30 дней, при необходимости курс терапии может быть проведен повторно, через 2-3 нед.
При выраженной интоксикации патогенетически оправданной является дезинтоксикационная инфузионная терапия глюкозо-солевыми растворами. В случае развития выраженной гипопротеинемии показано парентеральное введение раствора альбумина, плазмы.
Для купирования аллергического компонента болезни применяют антигистаминные неспецифические противовоспалительные препараты, которые рекомендуется использовать в течение всего периода проведения терапии противопаразитарными препаратами, так как распад гельминтов усиливает аллергические реакции организма пациента.
При тяжелых формах трихинеллеза, нейроцистицеркозе с признаками арахноидита, васкулита применяются глюкокортикостероиды (ГКС). Проведение ГКС-терапии приводит к нарушению процесса инкапсуляции личинок трихинелл в мышцах, которое обусловливает затяжное и рецидивирующее течение трихинеллеза. Развитие таких осложнений, как инфекционно-токсический шок, энцефалопатия, миокардит и т. д., является показанием к назначению ГКС. При миокардите преднизолон назначают в дозе 20-60 мг/сут до купирования основных клинико-лабораторных (глухость сердечных тонов, тахикардия, аритмия, расширение границ сердца, гиперферментемия) и электрокардиографических признаков осложнения [1].
В некурабельных ситуациях проводят хирургическое лечение. До проведения оперативного вмешательства больным эхинококкозом проводят курс этиотропной терапии. В случае наличия одиночной кисты под контролем УЗИ в полость вводят 95% этиловый спирт с мебендазолом (метод ПАИР: пункция-аспирация-инстилляция-реаспирация). Следует помнить о том, что извлечение кисты должно осуществляться без нарушения целостности кутикулярной оболочки и фиброзной капсулы. Резекцию части органа проводят при распространенном процессе. Поражение легких и костей при альвеококкозе также требует оперативного вмешательства. Применение албендазола повышает выживаемость больных после радикальной операции, его назначение также оправдано в неоперабельных случаях [4, 6, 14].
Диспансерному наблюдению подлежат все больные тканевыми гельминтозами. Необходимо помнить, что при токсокарозе контрольные клинические анализы крови и обследование методом ИФА с антигенами токсокар с интервалом 3-4 мес проводят после завершения этиопатогенетической терапии. Длительность диспансерного наблюдения – не менее 6 мес до получения двух отрицательных контрольных результатов. При трихинеллезе диспансерное наблюдение проводят в течение 6 мес. В случаях трихинеллезного миокардита и при наличии остаточных проявлений инвазии срок наблюдения продлевают до 1 года. Осмотр реконвалесцентов врачом-специалистом, исследование клинического анализа крови (при тяжелой форме – ЭКГ) выполняют через 2 нед, 2 мес, 5-6 мес после выписки из стационара. Больные эхинококкозом подлежат диспансерному наблюдению в течение 5-10 лет. При отсутствии признаков рецидива и стойко отрицательных серологических тестах больные могут быть сняты с учета. Пожизненной диспансеризации подлежат больные альвеококкозом. Периодичность и объем контрольных обследований те же, что и при эхинококкозе. При цистицеркозе кратность и объем наблюдения за реконвалесцентами определяется индивидуально, в зависимости от состояния функции пораженных органов.
К сожалению, паразитарные болезни часто оказываются последними в цепи дифференциально-диагностического мышления врача-гастроэнтеролога. Недооценивается значение гельминтозов, являющихся основной причиной патологии желудочно-кишечного тракта. Вот почему крайне важным является скрининг – тестирование пациентов с повышенными факторами риска паразитарной инвазии ввиду частого наличия гельминтов в печени, желчевыводящих путях, поджелудочной железе и кишечнике.
В целом следует отметить, что новые научные факты требуют переосмысления роли паразитарных инвазий в патологии человека, которая не исчерпывается традиционным представлением о патогенных гельминтах только как о возбудителях паразитарных болезней. Наличие этих паразитов приводит не только к развитию специфических клинических проявлений. За счет аллергизации и подавления иммунитета паразиты создают предпосылки к снижению эффективности вакцинопрофилактики и более частому возникновению других инфекционных и неинфекционных заболеваний. Стратегия и тактика химиотерапии должны быть направлены на предотвращение развития химиорезистентности, что достигается при использовании эффективных антигельминтиков. При назначении недостаточно эффективных препаратов в популяции гельминтов происходит отбор особей, имеющих резистентность к определенным препаратам или группе препаратов сходной химической структуры. Перспективы лечения гельминтозов заключаются в универсальной активности антигельминтного препарата в отношении чувствительных и резистентных форм паразитов, доказанной эффективности и позитивных результатах его применения.
Литература
- Антонов М.М., Антонова Л.П., Бабченко И.В. Тканевые гельминтозы у взрослых и детей (эпидемиология, клиника, диагностика, лечение, профилактика) // Метод. Рекомендации. – СПб., 2004. – 29 с.
- Возианова Ж.И. Инфекционные и паразитарные болезни. – 2007. – Т. 1. – 904 с.
- Кочергина Е.А., Корюкина И.П., Зубов Е.В. Особенности лечения паразитарных заболеваний // РМЖ. – 2004. – Т. 12, № 13.
- Лобзин Ю.В., Козлов С.С. Руководство по инфекционным болезням с атласом инфекционной патологии. – СПб.: Феникс, 2007. – 932 с.
- Лысенко А.Я., Владимова М.Г., Кондрашин А.В. Клиническая паразитология. – Женева, 2002. – С. 65-66.
- Онищенко Г.Г. Заболеваемость паразитарными болезнями в Российской федерации и основные направления деятельности по ее стабилизации // Медицинская паразитология. – 2002. – № 4. – С. 3-102.
- Сергеева В.П., Лобзина Ю.В., Козлов С.С. Паразитарные болезни человека (протозоозы и гельминтозы) // Руководство для врачей. – СПб., 2006. – 586 с.
- Bogoch I.I., Raso G., N'Goran E.K., Marti H.P., Utzinger J. Differences in microscopic diagnosis of helminths and intestinal protozoa among diagnostic centres // Eur. J. Clin. Microbiol. Infect. Dis. – 2006. – № 25 (5). – Р. 344-347.
- Correale J., Farez M. Association between parasite infection and immune responses in multiple sclerosis // Annals of Neurology. – Published Online: 17 Jan. 2007. http://elementy.ru/news/.
- Garg P.K., Perry S., Dorn M., Hardcastle L., Parsonnet J. Risk of intestinal helminth and protozoan infection in a refugee population // Am. J. Trop. Med. Hyg. – 2005. – № 73 (2). – Р. 386-391.
- Hokeleek M., Luwick L., Cua A. Nematode infections // Last Updated. – Jan. 17. –2003. – Medicine.com, Inc., 2004.
- Horton J. Treatment of parasitic diseases // Parasitology. – 2000. – S. 113-132.
- Hulda Regehr Clark. The Parasite Cleanse. – 2006. – http://www.curezone.com.
- Ross Anderson. ARE YOU CLEAR OF PARASITES? – 2006. – http://loaves-n-fishes.com.
- Stich A., Fleischer K. Worm infection. Intestinal helminthes // MMW Fortschr. Med. – 2001. – № 143 (14). – Р. 34-36.
- Stephen L. DrenchPlan // Primefact. – 2005. – № 14. – Р. 6-16.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Цирроз печени: насколько страшен диагноз…
Цирроз печени: насколько страшен диагноз…
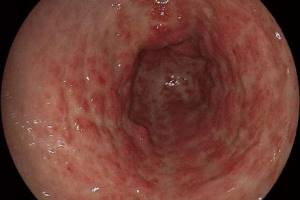 Основные причины кровотечений при заболеваниях печени
Основные причины кровотечений при заболеваниях печени
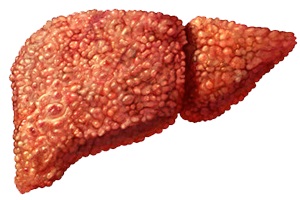 Цирроз печени
Цирроз печени
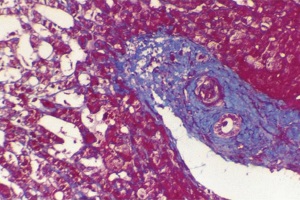 Нецирротический фиброз печени. Обзор литературы, клиническое наблюдение
Нецирротический фиброз печени. Обзор литературы, клиническое наблюдение