- Головна
- /
- Статті
- /
- Ендокринологія. Цукровий діабет
- /
- Осложнения сахарного диабета со стороны органа зрения
Осложнения сахарного диабета со стороны органа зрения
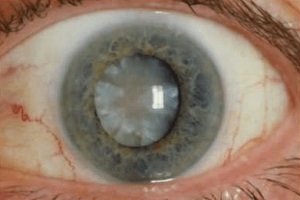
Мировая статистика последних лет свидетельствует о неуклонном росте заболеваемости сахарным диабетом (СД) среди населения нашей планеты. В связи с этим диабетическая ретинопатия (ДР), основное осложнение СД со стороны органа зрения, занимает лидирующее место среди известных причин слабовидения и слепоты, а число случаев утраты зрения в результате этого осложнения сохраняет устойчивую тенденцию к постоянному росту.
 Распространенность ДР определяет особое место среди известных медико-социальных проблем. По оценкам экспертов, ежегодно в мире примерно у 40 тыс. пациентов с СД появляются симптомы ДР.
Распространенность ДР определяет особое место среди известных медико-социальных проблем. По оценкам экспертов, ежегодно в мире примерно у 40 тыс. пациентов с СД появляются симптомы ДР.
Диабетическая ретинопатия, высокоспецифичное поражение сосудов сетчатки, в равной степени характерно и для инсулинзависимого, и инсулиннезависимого сахарного диабета. По мнению разных авторов, поражение сетчатки в разные сроки от начала заболевания развивается практически у 70-90% больных СД, причем среди пациентов с инсулинзависимым СД (ИЗСД) уже через 5-7 лет после постановки диагноза СД в 10% случаев появляются клинические признаки ДР, через 6-10 лет их число возрастает до 68%, через 20 – до 78%, через 30 лет 90% больных имеют различные по степени выраженности глазные осложнения. Частота встречаемости ДР и степень ее прогрессирования среди пациентов с инсулиннезависимым СД (ИНЗСД) выглядят несколько иначе, что, прежде всего, объясняется более поздним или несвоевременным выявлением СД, в результате чего практически через 5 лет после постановки диагноза признаки ДР обнаруживают не в 10% случаев, как при инсулинзависимом СД, а в 28%. Прослеживая динамику роста заболеваемости ДР, можно отметить, что при ИНЗСД она отличается меньшей склонностью к прогрессированию, вследствии чего ДР у больных с 30-летним стажем ИНЗСД выявляется примерно в 38% случаев, при ИЗСД – в 90%. Следует подчеркнуть, что слепота у больных диабетической ретинопатией развивается в 25 раз чаще, чем в общей популяции.
Патогенетические механизмы развития ДР достаточно разнообразны и до сих пор окончательно не изучены. Однако установлено, что в ее основе лежит микроангиопатия, как проявление генерализованного патологического процесса, развивающегося на уровне микрососудистой системы организма. Принято считать, что длительно неконтролируемый повышенный уровень глюкозы крови со значительными суточными перепадами является первопричиной таких сосудистых нарушений и ДР. В результате этого в первую очередь страдают клетки эндотелия и перициты сосудистой стенки, поскольку в них транспорт глюкозы осуществляется без участия инсулина. Связанные с гипергликемией морфофункциональные нарушения в перицитах способствуют атонии капилляров и развитию микроаневризм. Морфофункциональные и дегенеративные изменения эндотелиальных клеток приводят к образованию зон ограниченной капиллярной перфузии с последующей выработкой вазопролиферативного фактора, инициирующего активную пролиферацию патологических эндотелиальных клеток с утолщенной базальной мембраной, и так называемой неоваскуляризации. Все эти процессы инициируют развитие ишемии в ткани сетчатки, которая формируется в зонах капиллярной окклюзии при прогрессировании микроангиопатии, способствует развитию тежелых проявлений сосудистой декомпенсации сетчатки – отеку макулярной области и ДР.
Основой профилактики развития осложнений СД является компенсация углеводного обмена при постоянном контроле и коррекции АД и состояния функции почек. Принято считать, что уровень гликозилированного гемоглобина, как показателя компенсации СД, не должен превышать 7%.
Изучая классификацию ДР, можно сказать, что накопление сведений о клинике ДР происходило постепенно и еще в 1875 г. Leber предложил термин «ретинопатия» вместо ранее существовавшего «ретинит». Первые клинические описания диабетической ретинопатии представил Laeger в 1885 г.: наличие отека, пятен крови и мелких желтых очагов неправильной формы в ткани сетчатки. McKenzie в 1887-1889 гг. не только дал достаточно детальную характеристику ДР, но и отметил сходство изменений глазного дна при СД с изменениями в сетчатке при патологии почек. Он указал на специфичные для ДР признаки: сосудистые аневризмы и характерный геморрагический синдром. Практически в это же время W. Manz (1888) описал образование содержащих сосуды мембран, которые покрывали диск зрительного нерва и сетчатку, назвав их пролиферирующим ретинитом (Retinitis proliferans), а E. Nettleship – изменения вен при ДР, пролиферативную ретинопатию, неоваскулярную глаукому. Можно считать, что основы первых классификаций ДР были заложены в конце XIX века (Hirshberg, 1890).
В дальнейшем было предложено большое количество классификационных схем, отражавших уровень развития представлений о патогенезе диабетической ретинопатии, ее диагностике и лечении в соответствующие периоды времени. Одна из первых классификаций, адаптированных к лазерному лечению, опубликована H.C. Zweng и соавт. (1977). Авторы исходили из того, что существуют две независимые формы ДР: непролиферативная, характерная для пациентов пожилого возраста, и пролиферативная – для больных более молодого возраста. Затем F.L. Esperance и M. Davis (1977), М.Л. Краснов и М.Г. Марголис (1966), А.С. Ефимов (1973), Л.А. Кацнельсон (1979), В.П. Ивериели и Э.А.Чкония (1980), Л.Т. Кашинцева (1980), Л.Н. Ильков (1981), Л.И. Балашевич и Г.И. Авербах (1980), E. Kohner и М. Porta (1990), В.Ф. Экгардту (2001) представили свои варианты классификаций ДР. В литературе известна классификация ETDRS (1991, 2000), как результат независимых исследований по анализу диабетических осложнений со стороны органа зрения в виде оценки риска развития ДР и показаний для лазерной коагуляции сетчатки.
К сожалению, в Украине и сегодня не принята единая классификация ДР. Это связано с тем, что классификации изменений глазного дна у больных СД при постановке диагноза и при оказании различных видов специализированной медицинской помощи требуют разного уровня детализации или обобщения, которые учитывали бы и алгоритмы лечения той или иной стадии ДР.
В мировой практике наибольшее распространение получили классификации E. Kohner и М. Porta (1990) и ETDRS (1991, 2000).
Согласно классификации E. Kohner и М. Porta (1990) выделяют три стадии ДР:
- непролиферативную (микроаневризмы, редкие пятнистые геморрагии, твердые экссудаты, один-два мягких экссудата в сетчатке);
- препролиферативную (умеренную: изменение калибра и конфигурации вен, четкообразность, извитость, удвоение вен; средней тяжести: интраретинальные кровоизлияния в виде пятен, наличие твердых экссудатов (желтые, белые точки) по ходу крупных сосудов и в центральных отделах сетчатки, участки ишемии сетчатки в виде белых ватообразных очагов);
- пролиферативную (пролиферативная диабетическая ретинопатия, включающая новообразованные сосуды на диске зрительного нерва (ДЗН) в ткани сетчатой оболочки и в стекловидном теле, фиброз сетчатой оболочки, ретиновитреальные тракции).
Согласно этой классификации выделяют.
- Фоновую ДР (изменения на глазном дне отсутствуют)
- Непролиферативную диабетическую ретинопатию (НПДР):
- начальную;
- умеренную;
- среднетяжелую;
- тяжелую (препролиферативную).
- Пролиферативную диабетическую ретинопатию (ПДР):
- начальную;
- умеренную;
- тяжелую (высокого риска А и В);
- далеко зашедшую;
- исход.
Отдельно в классификации ETDRS выделено поражение центральной области сетчатки, или диабетическая макулопатия, и диабетический отек макулярной области (ДОМО):
- фокальный экссудативный макулярный отек;
- диффузный клинически значимый макулярный отек;
- ишемическая макулопатия;
- смешанные формы.
Это связано с тем, что появление ДОМО даже при отсутствии других клинических проявлений ДР само по себе представляет реальную угрозу для зрения при несвоевременном лечении больного СД.
Методы обследования больного СД включают: визометрию (проверку остроты зрения), переднюю и заднюю биомикроскопию глаза, периметрию поля зрения, кампиметрию (определение центрального поля зрения), тонометрию, гониоскопию (для определения неоваскуляризации в углу передней камеры), УЗИ глаза, оптическую когерентную томографию сетчатки (ОКТ), допплерографию сосудов глаза, фоторегистрацию глазного дна, флюоресцентную ангиографию (ФАГ).
В последнее время очень важным показателем гипоксии сетчатки и признаков отека макулярной области является толщина макулярной зоны (по данным ОКТ). Этот метод позволяет выявить доклинические проявления ДОМО. Раннее назначение соответствующей терапии способствует нормализации состояния глазного дна и является надежной профилактикой развития и прогрессирования ДР. Кроме того, этот высокоинформативный метод позволяет проводить на высоком уровне мониторинг состояния глазного дна и качества лечения. Сегодня этот метод считается неинвазивной альтернативой методу флюоресцентной ангиографии.
Для сохранения зрительных функций пациенту с сахарным диабетом необходимо постоянно наблюдаться у офтальмолога специализированного центра, который занимается данной проблемой. Только он может адекватно и грамотно определить показания к лечению (медикаментозному, лазерному или микрохирургическому). Следует учитывать, что любую терапию необходимо проводить при условии компенсации СД.
В Киевском городском центре сосудисто-эндокринных заболеваний органа зрения разработаны показания для направления пациентов с СД для консультации в специализированный центр.
- Необходимость проведения специального офтальмологического обследования (ОКТ макулярной области и зрительного нерва, ФАГ, УЗИ).
- Подозрение на отслойку сетчатки, отек макулярной области, повышение ВГД, свежее внутриглазное кровоизлияние (в порядке скорой помощи).
- Наличие отека макулы, видимое офтальмоскопически.
- Снижение остроты зрения при отсутствии офтальмоскопически видимых причин.
- Рубеоз радужки, обнаружение НВ в УПК при гониоскопии, появление гифемы.
- Повышение ВГД.
Регулярно наблюдаться у офтальмолога должны следующие пациенты:
- имеющие высокий уровень гликемии (HbA1с выше 10%), протеинурии – не реже одного раза в 6 месяцев даже при отсутствии изменений на глазном дне при первичном осмотре;
- при переводе на инсулинотерапию, так как в этом случае возможны перепады гликемии, что неблагоприятно сказывается на тканях и сосудистой системе глаза;
- при неожиданном снижении остроты зрения или появлении у больных сахарным диабетом каких-либо жалоб со стороны органа зрения, обследование должно быть проведено в порядке скорой помощи, независимо от планового осмотра офтальмологом.
Современные подходы к терапии ДР заключаются в строго по показаниям назначении медикаментозного, лазерного или микрохирургического лечения. Сегодня мы располагаем очень высокими технологиями, уникальной диагностической и микрохирургической аппаратурой, специалисты высокого уровня оказывают медицинскую помощь больным с диабетическими осложнениями со стороны органа зрения по современным мировым стандартам. Для достижения желаемого результата очень важно своевременно применить тот или иной подход, кроме того, при лечении ДР, как и других осложнений СД, исключительно важно достижение компенсации СД. Следует также помнить о таких постоянных факторах риска, как сопутствующие СД артериальная гипертензия и нефропатия.
Существует несколько основных направлений в лечении ДР.
- Лазерное лечение на стадиях непролиферативной и начальной пролиферативной ДР, при диабетической макулопатии (парамакулярный барраж, макулярная решетка, фокальная и панретинальная лазерокоагуляция сетчатки).
- Хирургическое лечение на стадиях ПДР, при тракционной отслойке макулярной области и рецидивирующем гемофтальме (эндовитреальное введение триамцинолона, закрытая витрэктомия с эндолазерокоагуляцией, с тампонадой газом и силиконом после удаления витреоретинального фиброза ретинальных мембран).
- Комбинированное микрохирургическое лечение вторичной декомпенсированной неоваскулярной глаукомы.
- Медикаментозная терапия (основная, фоновая).
Медикаментозная ДР остается достаточно эффективным методом лечения, и на нее в последние годы, несмотря на широкую распространенность ЛК и микрохирургии, специалисты все больше и больше обращают внимание. В медикаментозной терапии ДР широко используют ангиопротекторы, метаболиты, антиоксиданты, иммуномодуляторы, нейроретинопротекторы. Арсенал препаратов широк. Мы отрицательно относимся к назначению трентала, который практически у всех пациентов вызывает геморрагические внутриглазные осложнения, с осторожностью назначаем вазопростан, который у пациентов с ПДР и ДОМО может спровоцировать прогрессирование глазной патологии и усиление оттока МО. В нашей клинике все пациенты с СД обязательно получают медикаментозную терапию и как самостоятельное лечение, и в качестве фонового лечения при проведении ЛК или микрохирургического лечения. Такой подход значительно повышает эффективность лечения и удлиняет сроки стабилизации патологического процесса.
Контрастирование сосудов глазного дна при ФАГ
Результаты компьютерной когерентной томографии сетчатки
Глазное дно при умеренной НПДР (ETDRS)
Глазное дно при тяжелой ПДР (ETDRS)
Литература
- Балашевич Л.И. и соавт. Глазные проявления сахарного диабета. С-Пб. – 2004. – 382 с.
- Barrie P. Progress in diabetic maculopathy // Br J Ophthalmol. – 1999. – Vol. 43. – №1. – P. 3-8.
- Inoue M., Asumi A., Kajiura-Tsukahara Y., Yamamoto M. Ocular ischemic syndrome in diabetic patients // Jpn J Ophthalmol. – 1999. – Vol. 43. – №1. – P. 31-35.
- Kohner E.M. Diabetic retinopathy // Brit Med Bull. – 1978. – Vol. 5. – №1. – P. 148-173.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення



 Блефарит: воспалительное заболевание век
Блефарит: воспалительное заболевание век
 К вопросу о лечении заболеваний ЖКТ и билиарной системы
К вопросу о лечении заболеваний ЖКТ и билиарной системы  Дисфункции билиарной системы у детей
Дисфункции билиарной системы у детей
 Этиология, степень тяжести и лечение внебольничной пневмонии
Этиология, степень тяжести и лечение внебольничной пневмонии